
 2Al2O3的叙述中,正确的是( )
2Al2O3的叙述中,正确的是( ) 2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51.
2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51. 2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51,因此27g铝和24g氧气反应可生成51g氧化铝,故B错误;
2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51,因此27g铝和24g氧气反应可生成51g氧化铝,故B错误; 2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51,因此27g铝和24g氧气反应可生成51g氧化铝,故C正确;
2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51,因此27g铝和24g氧气反应可生成51g氧化铝,故C正确; 2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51,设和4g铝反应的氧气的质量是x,则
2Al2O3可知,参加反应的铝、氧气及生成的氧化铝的质量比为(27×4):(32×3):(102×2)=27:24:51,设和4g铝反应的氧气的质量是x,则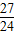 =
=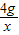 ,解得x=3.56g,因此4g铝和6g氧气反应可生成7.56g氧化铝,故D错误.
,解得x=3.56g,因此4g铝和6g氧气反应可生成7.56g氧化铝,故D错误.

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
(2013?柳州模拟)类推思维是化学解题中常用的一种思维方法,下列关于化学反应方程式的类推正确的是( )
|
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
 2Al2O3的叙述中,正确的是
2Al2O3的叙述中,正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com