
| A. | 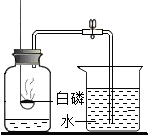 研究空气中氧气含量 | B. | 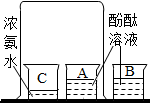 研究分子的运动 | ||
| C. | 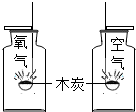 研究木炭在氧气中燃烧 | D. | 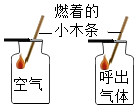 研究空气和呼出气体中氧气的含量 |
分析 对比实验可通过若干个装置同时探究一个或多个条件对同一事件的影响,其关键是必须至少有一组作为对照,据此进行分析解答.
解答 解:A.通过白磷燃烧消耗集气瓶中的氧气,测量进入集气瓶中水的体积可以测定空气中氧气的含量,根本不存在对比实验,没有利用对比实验的思想方法,故选项正确.
B.烧杯A中的酚酞试液和烧杯B中的酚酞试液属于对照试验,烧杯A置于放有浓氨水的烧杯附近;烧杯B置于空气中,没有变红色,说明空气不能使酚酞试液变红,烧杯A中变红说明氨分子在不断运动,进入烧杯A中,使酚酞试液变红,说明了分子在不断运动,利用了对比实验的思想方法,故选项错误.
C.研究木炭在氧气中燃烧,就是观察木炭在氧气中燃烧的现象以及产物的验证,根本不存在对照实验,没有利用对比实验的思想方法,故选项正确.
D.二氧化碳能使燃着的木条熄灭,空气能使燃着的木条正常燃烧,通过对比说明空气中氧气的含量高,利用了对比实验的思想方法,故选项错误.
故选:AC.
点评 本题难度不大,设计实验时要掌握其原理和区别,掌握对比实验的关键是必须至少有一组作为对照是正确解答本题的关键.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:填空题
 一根用细绳吊着的长玻璃棒左端绕上光亮的粗铜丝,并使玻璃棒保持水平(如图).用酒精灯给铜丝加热数分钟,停止加热后冷却,发现玻璃棒左端下降.用化学方程式表示左端下降的原因:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
一根用细绳吊着的长玻璃棒左端绕上光亮的粗铜丝,并使玻璃棒保持水平(如图).用酒精灯给铜丝加热数分钟,停止加热后冷却,发现玻璃棒左端下降.用化学方程式表示左端下降的原因:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
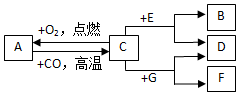 现有A~G七种常见物质,C和F都是最常见的金属,B是气体单质,D为含有氯离子的浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:
现有A~G七种常见物质,C和F都是最常见的金属,B是气体单质,D为含有氯离子的浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 稀盐酸的质量 | 剩余固体的质量 |
| 第1次加入5g | 1.315g |
| 第2次加入5g | 0.63g |
| 第3次加入5g | 0.40g |
| 第4次加入5g | 0.40g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入5g食盐 | B. | 蒸发掉45g水 | ||
| C. | 取出50g溶液 | D. | 加入50g 20%的食盐溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
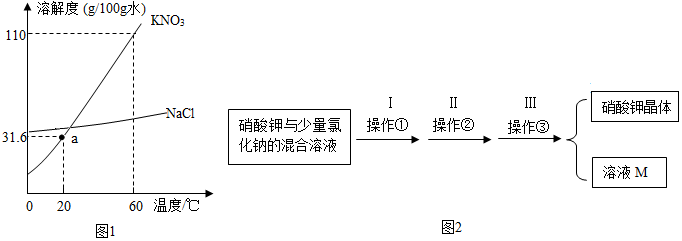
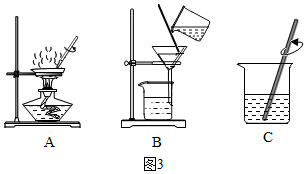
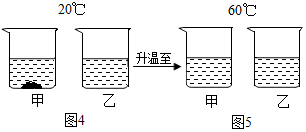
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com