硫酸钠与碳酸钠的固体混合物12.2克(均不含结晶水)可以跟150克硫酸溶液恰好完全反应生成正盐,同时生成2.2克气体.计算:
(1)固体混合物中碳酸钠的质量是多少?
(2)反应完毕所得溶液的溶质质量分数是多少?
【答案】
分析:固体混合物中碳酸钠与硫酸反应硫酸钠、水同时放出气体二氧化碳而硫酸钠与硫酸不反应,最终所得溶液为硫酸钠溶液,溶液中硫酸钠由混合物中的硫酸钠和反应生成的硫酸钠两部分组成部分;因此可根据生成气体二氧化碳的质量,利用反应的化学方程式,计算出混合物中碳酸钠的质量和生成硫酸钠的质量,即可解决问题.
解答:解:设混合物中碳酸钠的质量为x,生成硫酸钠的质量为y
Na
2CO
3+H
2SO
4=Na
2SO
4+H
2O+CO
2↑
106 142 44
x y 2.2g
106:44=x:2.2g 解之得 x=5.3g
142:44=y:2.2g 解之得 y=7.1g
则原混合物中硫酸钠的质量为12.2g-5.3g,溶液中最终含有的硫酸钠质量为12.2g-5.3g+7.1g.
溶液的总质量为反应物的全部减去生成的气体,即12.2g+150g-2.2g.
所以反应完毕所得溶液的溶质质量分数=
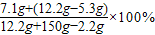
=8.75%
答:(1)固体混合物中碳酸钠的质量是5.3g;
(2)反应完毕所得溶液的溶质质量分数是8.75%.
点评:根据质量守恒定律,反应后溶液的质量=固体混合物的质量+稀硫酸的质量-生成气体的质量.

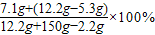 =8.75%
=8.75%
