
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 25.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
分析 (1)根据表格提供的数据来分析;
(2)由20℃时硝酸钾的溶解度为31.6g,判断60℃时200gKNO3溶液中含溶质 100g,将该溶液降温至 20℃,可析出KNO3质量.
(3)根据物质的溶解度受温度的影响来分析.
解答 解:(1)由表格提供的硝酸钾的溶解度可知,20℃时KNO3的溶解度是31.6g;故填:31.6;
(2)60℃时,200gKNO3溶液中含溶质100g,则含有溶剂水的质量为200g-100g=100g,而20℃时KNO3的溶解度是31.6g,所以降温至20℃时析出晶体的质量为:100g-31.6g=68.4g;故填:68.4;
(3)氯化钠的溶解度受温度的影响不大,硝酸钾的溶解度受温度的影响变化较大,NaCl溶液中含有少量KNO3,提纯NaCl,采用蒸发溶剂结晶法.故填:蒸发结晶.
点评 本题难度不大,掌握理解溶解度的概念、结晶的方法并能灵活运用是正确解答本题的关键.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
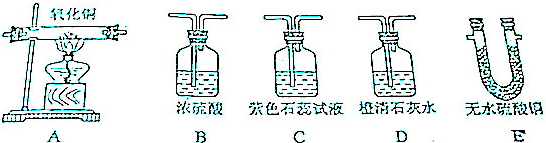
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
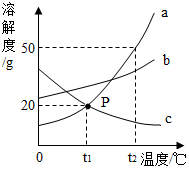 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com