
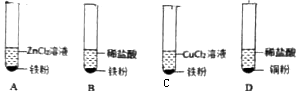
分析 铁和稀盐酸反应生成氯化亚铁和氢气;
氯化亚铁溶液是浅绿色溶液,氯化铁溶液是黄色溶液.
解答 解:(1)A中无明显现象,说明锌比铁活泼,B中产生气泡,溶液由无色变成浅绿色,说明铁和稀盐酸发生了反应,进一步说明铁比氢活泼,D中无明显现象,说明氢比铜活泼,由ABD可以判断锌比铁活泼,铁比氢活泼,氢比铜活泼,因此为达到实验目的,可以省略的实验是C.
故填:C.
(2)将C试管反应后的混合物过滤,向滤渣中加稀硫酸,有气泡产生,说明铁过量,则滤液中的溶质为氯化亚铁.
故填:氯化亚铁.
(3)B试管中铁粉和过量的稀盐酸反应后,长期敞放在空气中,氯化亚铁能被氧化成氯化铁,会观察到的现象是溶液由浅绿色变成黄色.
故填:溶液由浅绿色变成黄色.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.


科目:初中化学 来源: 题型:选择题
| A. | SO42-、Cl-、Na+、H+ | B. | K+、SO42-、Cu2+、NO3- | ||
| C. | Cl-、K+、SO42-、Na+ | D. | Ca2+、Na+、CO32-、Cl- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然界中甲元素只以化合物形式存在,乙元素有单质形式存在 | |
| B. | 甲能与盐酸反应而乙不能 | |
| C. | 甲能从乙的盐溶液中置换出乙 | |
| D. | 化合物中甲元素显+2 价而乙元素显+3 价 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 消毒液1000毫升 | |
| 溶质的质量分数 | 25% |
| 密度 | 1.2克/厘米3 |
| 相对分子质量 | 74.5 |
| 腐蚀性;致敏性;游离氯可能引起中毒 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com