
 某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:
某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:分析 碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,反应前后的质量差即为反应生成碳酸钙的质量,再根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)反应生成沉淀的质量m为:11g+100g+141g-242g=10g,
故填:10.
(2)设碳酸钠质量为x,反应生成氯化钠质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
x 10g y
$\frac{106}{x}$=$\frac{100}{10g}$=$\frac{117}{y}$,
x=10.6g,y=11.7g,
纯碱样品中含有氯化钠的质量为:11g-10.6g=0.4g,
故填:0.4.
(3)滤液中溶质的质量分数为:$\frac{11.7g+0.4g}{242g}$×100%=5%,
答:滤液中溶质的质量分数为5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题
 不少科学家认为地球表面变暖及一些异常气候(如年初发生在我国南方部分地区的雪灾)与大气中二氧化碳的含量增加所形成的“温室效应”有一定的关系.
不少科学家认为地球表面变暖及一些异常气候(如年初发生在我国南方部分地区的雪灾)与大气中二氧化碳的含量增加所形成的“温室效应”有一定的关系.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
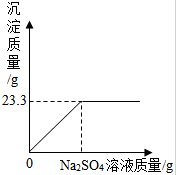 称取NaCl和BaCl2的固体混合物31.3g,加入100g蒸馏水,完全溶解后,向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示,试回答下列问题:
称取NaCl和BaCl2的固体混合物31.3g,加入100g蒸馏水,完全溶解后,向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示,试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示.
在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛应用于玻璃、造纸等的生产.将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应
已知A、B、C、D、E均为初中化学常见的酸、碱、盐.其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛应用于玻璃、造纸等的生产.将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应查看答案和解析>>
科目:初中化学 来源: 题型:解答题
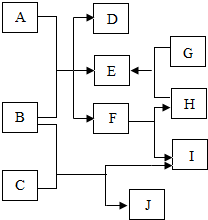 如图中A~J均为初中化学中的常见物质,其中仅C、H、I为单质.A为大理石的主要成分.J由两种元素组成,且其溶液为浅绿色.(反应条件均已省略)
如图中A~J均为初中化学中的常见物质,其中仅C、H、I为单质.A为大理石的主要成分.J由两种元素组成,且其溶液为浅绿色.(反应条件均已省略)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com