
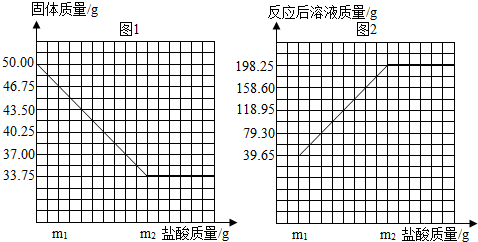
(7分)普通黄铜由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件等。为了测定某黄铜样品中铜的含量,设计了如下实验方案。取50.00g黄铜样品,加入一种未知浓度的稀盐酸。有关实验数据如下图。


(1)样品完全反应产生H2的质量___________。
(2)图中m与n的关系是m n(填“>”、“<”或“﹦”)。
(3)黄铜样品中铜的质量分数是多少(写出计算过程,保留小数点后一位)。
(4)某同学根据图中数据计算盐酸的溶质质量分数为:

请分析该同学的计算结果是否正确,如不正确指出错误的原因: 。(2分)
 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| m(HCl) |
| m(HCl溶液) |
| m(HCl) |
| 198.25-m(zn) |
查看答案和解析>>
科目:初中化学 来源: 题型:

| m(HCl) |
| m(HCl溶液) |
| m(HCl) |
| 198.25-m(zn) |
查看答案和解析>>
科目:初中化学 来源: 题型:

| m(HCl) |
| m(HCl溶液) |
| m(HCl) |
| 198.25-m(Zn) |
查看答案和解析>>
科目:初中化学 来源:2013年江苏省盐城市中考化学最后一次模拟试卷(解析版) 题型:解答题

 ×100%=
×100%= ×100%=10.03%请分析该同学的计算结果是否正确,如不正确指出错误的原因:______.
×100%=10.03%请分析该同学的计算结果是否正确,如不正确指出错误的原因:______.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com