
人体内的一些液体正常pH范围如下,其中呈酸性的是
A. 血浆7.35-7.45 B. 胆汁7.1-7.3
C. 胃液0.9-1.5 D. 胰液7.5-8.0
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源:2020年河南省南阳市淅川县中考一模化学试卷 题型:单选题
推理是化学学习中常用的思维方法,下列推理正确的是
A. 铁能将铜从硫酸铜溶液中置换出来,因此银也能将铜从硫酸铜溶液中置换出来
B. 物质燃烧需要同时满足三个条件,因此灭火也需要同时破坏这三个条件
C. 碱溶液的pH>7,因此测得某溶液的pH=12,该溶液一定是碱溶液
D. NaOH溶液中OH﹣能与酸反应,因此KOH溶液中的OH﹣也能与酸反应
查看答案和解析>>
科目:初中化学 来源:2020年天津市红桥区中考三模化学试卷 题型:填空题
水及溶液与人类的生活生产密切相关。根据下列图示,请回答相关问题。
图1活性炭净水器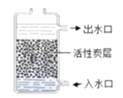 图2 水的电解
图2 水的电解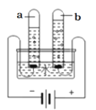
图3 溶解度曲线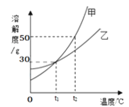 图4 探究实验
图4 探究实验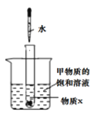
(1)图1中,活性炭净水器主要利用了活性炭具有的____性;图2所示实验中,试管b中得到的气体是(写物质名称)____。
(2)图3为甲、乙两种固体物质的溶解度曲线图。t1℃时,甲物质的溶解度是__,t2℃时,甲的饱和溶液溶质质量分数_________乙的饱和溶液溶质质量分数(填“大于”、“等于”、“小于”之一);图4所示实验中,将水滴入盛有物质X的小试管中,可观察到烧杯中有甲物质的固体析出。则物质X可能是_________(填序号之一)。
A 食盐 B 烧碱 C 生石灰 D 硝酸铵
(3)下图是氯化钠和硝酸钾在不同温度的溶解度,请回答。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
①20℃时,将136g饱和NaCl溶液蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为____;
②某小组想用20%的氯化钠溶液(密度为1.17g/cm3),配制30g质量分数为10%的氯化钠溶液,需要20%的氯化钠溶液____mL。(计算结果精确到0.1)
③若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是___(填序号)。
A 0~20℃ B 20~40℃ C 40~60℃ D 60~80℃
查看答案和解析>>
科目:初中化学 来源:2020年天津市红桥区中考三模化学试卷 题型:单选题
某同学梳理归纳了以下知识:①硬水通过活性炭吸附后可变为软水②“粗盐提纯”的实验中,当蒸发皿中出现较多固体时,停止加热③离子是带电的粒子,带电的粒子不一定是离子④氢氧化钠能去除油污,可作炉具清洁剂 ⑤为了防止天然气泄漏,在燃气灶下方安装报警器⑥取一小块乒乓球碎片和滤纸碎片,放在酒精灯火焰上加热,则滤纸先燃烧;以上说法不正确的是
A.①④⑥ B.①②④ C.②③⑥ D.①⑤⑥
查看答案和解析>>
科目:初中化学 来源:2020年天津市红桥区中考三模化学试卷 题型:单选题
2019年10月1日,北京天安门前举行了盛大的国庆70周年阅兵仪式。下列情景中蕴含着化学变化的是:
A.彩旗飘扬 B.气球升空 C.燃放礼花 D.声音远扬
查看答案和解析>>
科目:初中化学 来源:2020年湖南省常德市澧县中考模拟化学试卷 题型:填空题
在“生石灰、明矾、碳酸钙、不锈钢、聚乙烯、纯碱”中选择适当的物质填空。
(1)用于制造医疗器械、炊具的是_______;(2)用作食品干燥剂的是_________;
(3)用于造纸、纺织工业的盐是________;(4)用作补钙的盐是_____________;
(5)属于有机高分子化合物的是________;(6)净化水时可作絮凝剂的是_____。
查看答案和解析>>
科目:初中化学 来源:2020年江苏省连云港市灌南县新知双语学校中考模拟化学试卷 题型:流程题
过氧化钙( CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH)2,含少量CaCO3]为原料制备CaO2的一种工艺流程如下:

(查阅资料)I. Ca(OH)2+2NH4Cl=CaCl2+2NH3·H2O
Ⅱ.CaCl2+2NH3·H2O+H2O2 +6H2O= CaO2·8H2O↓+ 2NH4Cl
Ⅲ. CaO2·8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是_______;Ca(OH)2的俗名为_______;“过滤1”所得滤渣的主要成分是_______。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边缘略低于漏斗口、_______。生产过程中为了精确测定溶液的pH,常使用_______ (填仪器名称)。
(3)在其他条件不变的情况下,制备CaO2·8H2O的反应时间(t)对其产率(w)的影响如图所示。

①平均反应速率最快的时间段为:_______ (填字母)。
a. 0~10min b. 10~20min c. 20~30min d.30~40min
②30min后,w开始下降的主要原因是_______。
(4)为了测定加入的NH4Cl溶液中溶质的质量分数,取30.00g NH4Cl溶液于烧杯中,加入稍过量的AgNO3溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过计算确定该溶液中NH4Cl的质量分数(精确到0.1%)____。
查看答案和解析>>
科目:初中化学 来源:2020年云南省红河州弥勒市中考二模化学试卷 题型:计算题
氧化亚铜(Cu2O)可用作制造陶瓷着色剂(红色)、船底涂料等。现将Cu2O和Cu的固体混合物30g放入烧杯中,加入质量分数为19.6%的稀硫酸100g,恰好完全反应。请计算: (提示: 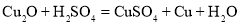 )
)
(1)所加稀硫酸中溶质的质量为 g。
(2)原混合物中Cu2O的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com