
| A.Zn与盐酸反应 | B.NaOH固体溶于水 |
| C.铁粉生锈 | D.NH4NO3固体溶于水 |
科目:初中化学 来源: 题型:阅读理解


| 影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
| ①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中. | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II. | 锈蚀的速率I<II;铁的锈蚀速率与反应时的温度有关, 温度越高,铁的锈蚀速率越快 温度越高,铁的锈蚀速率越快 . |
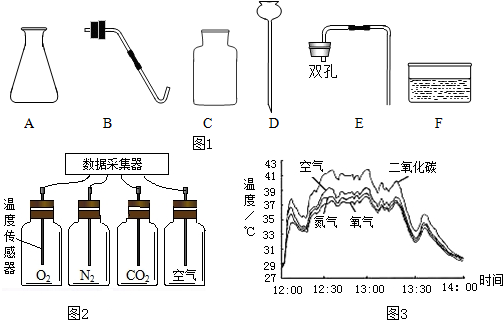
| ②氧气含量 | 在相同温度下,向I、II两套装置的集气瓶中分别通入氧气和空气. 在相同温度下,向I、II两套装置的集气瓶中分别通入氧气和空气. |
铁钉均锈蚀,且U型管中液面由b处上升至a处所需时间I<II. 铁钉均锈蚀,且U型管中液面由b处上升至a处所需时间I<II. |
铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快. |
| ③水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇. | 两套装置中铁钉均锈蚀; 且U型管中液面均由b处上升至a处,则所需时间I<II. |
铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快. 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
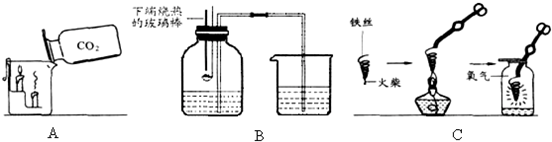
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
(未填) |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2012?天桥区三模)为了验证质量守恒定律,在两个小试管中分别注入20g 4.9%稀硫酸和20g氯化钡溶液,放于一个大烧杯中称量,如图所示.试根据要求,回答下列问题:
(2012?天桥区三模)为了验证质量守恒定律,在两个小试管中分别注入20g 4.9%稀硫酸和20g氯化钡溶液,放于一个大烧杯中称量,如图所示.试根据要求,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com