
【题目】化学与生活密切相关,回答下列问题:
(1)用于烘焙糕点的![]() 俗称为________________;
俗称为________________;
(2)鸡蛋和牛奶都富含的人体需要的营养素是________________;
(3)铁制品容易生锈的环境是______________________________;
(4)关闭煤气开关灭火的原理是____________________________;
 科学实验活动册系列答案
科学实验活动册系列答案科目:初中化学 来源: 题型:
【题目】酸、碱、盐是三类重要物质.
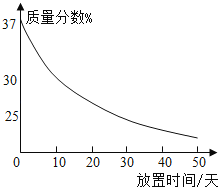
(1)实验室中有一瓶敞口放置的浓盐酸.它的质量分数和放置天数的关系如图.假设水不蒸发,分析浓盐酸的溶质质量分数变化的原因_____.
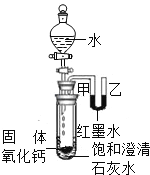
(2)观察图片,向小试管内滴加水后,除看到氧化钙固体溶解外,还可观察到的现象是_____.解释产生此现象的原因_____;_____.
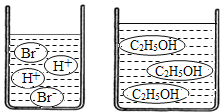
(3)如图分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图.请你结合已有的酸、碱知识,判断溴化氢的水溶液显_____,乙醇的水溶液显_____(填“酸性”、“中性”或“碱性”).
(4)向盛有10mL稀盐酸(其中滴有少量指示剂)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下.请分析并回答下列问题:
加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.5 | 7.0 | 11.0 | 12.0 |
①若滴加的指示剂是紫色石蕊溶液,当加入氢氧化钠溶液的体积为13mL时,溶液显_____色.
②若滴加指示剂是无色酚酞溶液,入氢氧化钠溶液充分振荡后,溶液颜色无变化.此时溶液中的溶质一定有(填化学式)_____;可能有_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应的实验或事实的是( )
A.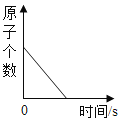 硫在密闭容器内燃烧,容器内原子个数随时间变化的关系
硫在密闭容器内燃烧,容器内原子个数随时间变化的关系
B.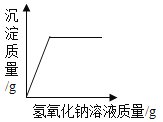 向硫酸铜和稀硫酸的混合溶液中不断加入氢氧化钠溶液
向硫酸铜和稀硫酸的混合溶液中不断加入氢氧化钠溶液
C.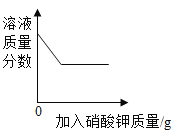 20℃时,向一杯不饱和硝酸钾溶液中逐渐加入硝酸钾晶体
20℃时,向一杯不饱和硝酸钾溶液中逐渐加入硝酸钾晶体
D.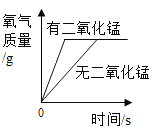 两份完全相同的过氧化氢溶液在有无
两份完全相同的过氧化氢溶液在有无![]() 情况下的反应
情况下的反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:

已知相关物质的溶解度(20℃)如下表:
物质 | K2CO3 | K2SO4 | KMnO4 |
溶解度/g | 111 | 11.1 | 6.34 |
(1)KMnO4中锰元素的化合价为_____.
(2)操作I的名称是_____.“干燥”过程中温度不宜过高的原因是_____(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MnO4+2CO2═2KMnO4+MnO2↓+2K2CO3;不用稀H2SO4酸化,反应的化学方程式为:3K2 MNO4+2H2SO4═2KMnO4+MnO2↓+2K2SO4+2H2O;工业上不采用稀H2SO4酸化的原因是_____.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:2K2 MnO4+2H2O![]() 2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是_____.
2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室要配制100g质量分数为16.5%的![]() 溶液,回答问题:
溶液,回答问题:
(1)计算:需要称取![]() ________g;
________g;
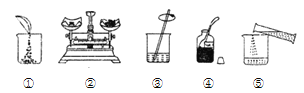
(2)图③操作中,用玻璃棒搅拌的作用是________________;
(3)量取水时最好选择________(选填“10mL”或“50mL”或“100mL”)的量筒
(4)若按图②操作配制溶液时,浓度偏差与下列________情况相同。
A 中有少量不溶性杂质 B. 量取水时仰视读数
C 量取水时俯视读数 D 装瓶时洒出来
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以工业大理石(主要杂质是氧化铁)为原料提纯碳酸钙的流程如下:
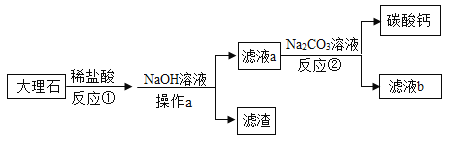
(1)为加快反应①中的速率,可采取的措施是_____________________
(2)操作a的名称为___________,在实验室里进行此操作,将滤纸紧贴漏斗内壁的原因是__________________。
(3)写出反应②的化学方程式________________,其基本反应类型是____________________。
(4)碳酸钙在生活、生产中有着广泛的应用,请写出一种碳酸钙在生活中的用途________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校兴趣小组的同学,利用实验室的氯化钠配制一定质量分数的氯化钠溶液。
(1)同学们发现实验室的氯化钠中含有不溶性杂质,在配制溶液前先进行提纯,粗盐提纯的操作步骤有溶解、过滤、_______、计算产率。其中一组同学将10g粗盐进行提纯,提纯后恰好配制成1000g溶质质量分数为0.9%的氯化钠溶液,则提纯过程中精盐的产率为_______。
(2)另一实验小组的同学,利用提纯后的氯化钠进行了如下实验。
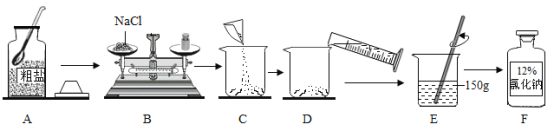
请根据示意图回答:
①上述操作中,有错误的是_______(填字母)。
②通过计算可知,托盘天平左盘中固体氯化钠的质量应为_______g;在称量氯化钠的过程中,同学发现托盘天平的指针偏向右盘,应_______(填字母);
增加氯化钠固体
减少氯化钠固体
调节平衡螺母
③操作E中,玻璃棒的作用是_______。
④下列情况可能会造成所配制溶液中溶质的质量分数偏小的是_______(填字母)。
A 得到的![]() 未完全干燥 B 用量筒量取水时,仰视读数 C 配好的溶液装瓶后,烧杯内有溶液残留
未完全干燥 B 用量筒量取水时,仰视读数 C 配好的溶液装瓶后,烧杯内有溶液残留
(3)其他小组想用12%的氯化钠溶液(密度为![]() ),配制20g质量分数为6%的氯化钠溶液,需要12%的氯化钠溶液_______mL(计算结果精确到0.1)
),配制20g质量分数为6%的氯化钠溶液,需要12%的氯化钠溶液_______mL(计算结果精确到0.1)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)家中蒸馒头用的纯碱中含有氯化钠,某实验小组要测定该纯碱中碳酸钠的质量分数。取6 g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡,此时烧杯中没有不溶物,其消耗稀盐酸61.7 g,测得反应后溶液的质量为65.5 g。请帮助实验小组完成以下计算:
(1)样品中碳酸钠的质量分数是多少?(计算结果保留至0.1%)
(2)反应后溶液中溶质的质量分数是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com