
【题目】实验室有大理石、稀盐酸、棉花,相关仪器及用品:
(1)补充一种药品在实验室可制取氧气,反应的化学方程式为___;

(2)实验室用由A→C的装置制备并探究二氧化碳的性质,请将A、C两部分实验装置图补充完整____;A中仪器a的用途是___;
(3)B中观察到的现象是______,产生现象的原因是____,使A中气体增多,气压増大,______,在压强差的作用下,气体进入B中,______,产生上述现象.由C中现象得出二氧化碳的物理性质是_____.
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑  随时添加液体药品 导管口有气泡冒出,澄清石灰水变浑浊 碳酸钙和盐酸反应生成氯化钙、水和二氧化碳 锥形瓶内的气压大于外界大气压 二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水 二氧化碳的密度比空气大
随时添加液体药品 导管口有气泡冒出,澄清石灰水变浑浊 碳酸钙和盐酸反应生成氯化钙、水和二氧化碳 锥形瓶内的气压大于外界大气压 二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水 二氧化碳的密度比空气大
【解析】
(1)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)A装置中的长颈漏斗应该伸入液面以下,防止生成的气体从长颈漏斗逸出,C装置中导管位于烧杯口附近,所以

A中仪器a的用途是:随时添加液体药品;
(3)B中观察到的现象是导管口有气泡冒出,澄清石灰水变浑浊,产生现象的原因是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,使A中气体增多,气压増大,锥形瓶内的气压大于外界大气压,在压强差的作用下,气体进入B中,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,产生上述现象.由C中现象得出二氧化碳的物理性质是二氧化碳的密度比空气大.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:初中化学 来源: 题型:
【题目】工业上用甲和乙反应制备丙和丁,其反应的微观示意图如图:
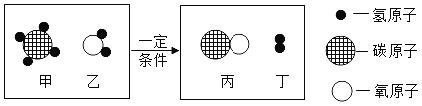
(1)写出该反应的化学方程式_____;
(2)该化学变化中没有发生改变的粒子是_____(填“分子”或“原子”);
(3)该反应中含氢元素的化合物有_____种;反应前后化合价发生变化的元素是_____(填元素符号).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了解某NaCl、Na2CO3固体混合物中Na2CO3与盐酸的反应情况,张南同学取16g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下表中相关数据,请分析表格中数据,回答下列问题。
加入稀盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
烧杯及反应后混合物的总质量/g | 122.2 | 146.1 | 170.0 | 193.9 | 218.9 |
(1)写出发生反应的化学方程式___;
(2)列出求解该混合物中碳酸钠质量(x )的比例式___;
(3)前三次加酸后参加反应碳酸钠质量占原混合物中碳酸钠质量的百分比为___;
(4)当加入稀盐酸至固体混合物恰好完全反应时,若向所得不饱和溶液中加入59.4g蒸馏水,最终所得溶液中溶质的质量分数是___;
(5)若用36.5%的浓盐酸配制上述所需要的盐酸,则需要加水的质量为___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图中A、B、C三种物质(均不含结晶水)的溶解度曲线,回答下列问题:

(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_____。
(2)t2℃时,向100g水中加入20gA物质,充分溶解后,所得溶液是_____(填“饱和”或“不饱和”)溶液。
(3)t3℃时,等质量的A、B饱和溶液分别降温至t2℃,对所得溶液的叙述正确的是_____(填序号)
①溶质质量:A>B ②溶剂质量:A<B ③溶质质量分数:A=B
(4)A中含有少量B,应采用_____的方法提纯A.(填“降温结晶”或“蒸发结晶”)。
(5)将t3℃时,A、B、C三种物质中的饱和溶液降温到t2℃时,A、B、C三种物质的溶质质量分数由小到大的顺序是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化铜与氢氧化铜的混合物25.8g,加入稀盐酸恰好完全反应得到325.8g溶液,将溶液结晶得到40.5g的固体。稀盐酸中氢元素的质量分数为( )
A. 0.2%B. 10.3%C. 10.5%D. 10.6%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器中有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
物质 | X | Y | Z | Q |
反应前质量/g | 4 | 10 | 1 | 21 |
反应前质量/g | 0 | 12 | 15 | 待测 |
已知X的相对分子质量为n,Q的相对分子质量为2n,则下列推断正确的是( )
A. 反应后Q的质量为10g
B. 反应式中X与Q的化学计量数比为2:3
C. 反应后生成15gZ
D. 反应中Y与Q发生改变的质量比为1:6
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为几种固体的溶解度曲线,回答下列问题:

(1)NaCl的溶解度随温度变化的规律是_____;
(2)_____℃时KNO3和KCl的溶解度相等;
(3)50℃时,KCl溶液的最大浓度(列式即可)为_____;
(4)60℃时,10g NaCl和90g KNO3完全溶解于100g蒸馏水,冷却到20℃后,_____(“有”或“没有”)NaCl析出,有_____gKNO3结晶析出。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com