
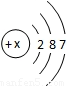 ;则x=______.根据元素原子结构示意图,不能直接获得的信息是______(填编号).
;则x=______.根据元素原子结构示意图,不能直接获得的信息是______(填编号). 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:阅读理解
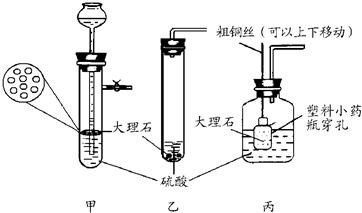
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源:2010年专题突破训练:计算题(解析版) 题型:解答题
| 化学纯硫酸 化学式:H2SO4 溶质质量分数:98.0% 密度:1.84g/mL 体积:500mL |
查看答案和解析>>
科目:初中化学 来源:2010年天津市北辰区中考化学模拟试卷(解析版) 题型:解答题
| 化学纯硫酸 化学式:H2SO4 溶质质量分数:98.0% 密度:1.84g/mL 体积:500mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com