
过氧化钙(CaO2)具有较强的漂白、杀菌消毒作用,对环境无危害,是一种很有应用价值和发展前途的化工产品.工业上利用双氧水和氢氧化钙制备CaO2,已知:双氧水高温下不稳定、会分解.下图是简化后的工艺流程,请回答下列问题.
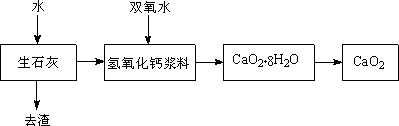
(1)生石灰中加水发生的化学反应方程式是________,该反应是________反应(填“放热”或“吸热”).在加入双氧水前,氢氧化钙浆料需经过________处理(填“保温”、“升温”、“降温”)处理.
(2)氢氧化钙浆料中加入双氧水的反应属于化合反应,则反应方程式为________,获得的产品CaO2·8H2O的相对分子质量为________,其中Ca、O、H的元素质量比为________.
(3)CaO2常用于鱼虾运输过程中的供氧剂,其反应原理是:2CaO2+2________=2Ca(OH)2+O2↑,若需要提供12.8 g氧气,则需要CaO2________g.Na2O2也能与水反应原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析其原因________.
答案:(1)CaO+H2O=Ca(OH)2 放热,降温;(2)Ca(OH)2+H2O2+6H2O=CaO2?8H2O,216,40:160:16;(3)H2O,57.6,因Na2O2与水反应生成的NaOH有强碱性,不利于鱼虾生存.
| 144 |
| 32 |
| x |
| 12.8g |


 计算高手系列答案
计算高手系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| 实验装置 | 实验主要 |
 |
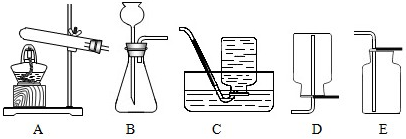
①检查装置气密性:先将导管口伸入水面下,用受紧握试管,观察到 导管口有气泡冒出 导管口有气泡冒出 ,松开后,有少量水进入导管.②将适量过氧化钙加入试管中,加入,导管口有大量气泡冒出. ③收集一瓶气体并检验气体. ④停止加热,熄灭酒精灯前,应 先将导管从水槽中移出来 先将导管从水槽中移出来 . |
| 实验装置 | 实验主要过程 |
| 该实验的发生装置应选择 B B ,收集装置可选择C C 或E E .(填序号) |
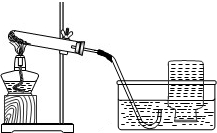
①检验装置气密性. ②将水加入过氧化钙中,有少量细小气泡缓慢放出,该装置放置到第二天,集气瓶中只收集到极少量气体,震荡发生装置仍有少量细小气泡缓慢放出. |
查看答案和解析>>
科目:初中化学 来源: 题型:
(6分)
长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
(1)提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢?
(2)进行猜想:甲同学认为:生成氧化钙和氧气;
乙同学认为:生成氢氧化钙[Ca(OH)2]和氧气。
你认为 同学的猜想是错误的,其理由是 。
(3)设计实验:验证另一个同学的猜想是正确的,并填入下表空格中。
| 实验方法 | 实验现象 | 实验结论 |
| ①取少量过氧化钙放入试管中,加足量水,将带火星的木条伸进试管中。 |
| 有氧气生成 |
| ②取实验①静置后的上层清夜, 。 |
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com