
【题目】取氯化钙和氯化钠的混合物10g,加入40g水使其完全溶解,再加入50g碳酸钠溶液恰好完全反应,过滤,得95g滤液(不考虑实验过程中质量损失),计算:
(1)所加碳酸钠溶液的溶质质量分数;
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%).
【答案】(1)10.6%;(2)10.8%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了碳酸钙,所以可以求算碳酸钙的质量,根据碳酸钙和对应的化学方程式求算碳酸钠和生成氯化钠的质量,进而求算对应的质量分数.
(1)根据质量守恒定律可得,生成的碳酸钙的质量为10g+40g+50g﹣95g=5g
设碳酸钠的质量为x,样品中氯化钙的质量为y,生成的氯化钠的质量为z.
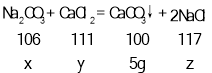
![]()
x=5.3g
y=5.55g
z=5.85g
碳酸钠溶液中碳酸钠的质量分数为![]() ×100%=10.6%
×100%=10.6%
(2)反应后所得溶液中氯化钠的质量分数为![]() ×100%≈10.8%
×100%≈10.8%
答:(1)所加碳酸钠溶液的溶质质量分数为10.6%;
(2)反应后所得滤液中溶质的质量分数约为10.8%.


科目:初中化学 来源: 题型:
【题目】如图是初中化学常见物质的相互转化关系示意图.其中A是一种金属氧化物.
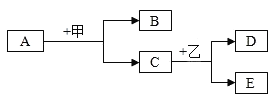
请回答下列问题:
(1)若甲是稀硫酸,D为蓝色沉淀,则D为_____,A为_____.写出A跟甲反应的化学方程式_____.
(2)若乙是稀硫酸,A为红色固体,写出C跟乙反应的化学方程式_____.若B能使澄清石灰水变浑浊,写出B与石灰水反应的化学方程式_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有实验室有一包白色粉末,可能含有![]() 和
和![]() 中的一种或几种,为了确定其成分,某化学兴趣小组进行了如下探究。
中的一种或几种,为了确定其成分,某化学兴趣小组进行了如下探究。
(查阅资料)![]() 固体不溶于水,也不溶于稀盐酸。
固体不溶于水,也不溶于稀盐酸。
(实验探究)
(1)甲同学设计了如下的实验方案。
实验步骤 | 实验现象 | 实验结论 |
a取少量该粉末于试管中,加入足量水充分溶解 | 有白色沉淀 | 有原粉末中一定含有 |
b将步骤a试管中物质过滤,向滤液中滴加酚酞溶液 | 溶液变红 | 原粉末一定含有_______ |
(2)乙同学认为甲同学步骤a的结论不一定正确,其理由是_______,他补充了如下实验,取白色沉淀于试管中,加入足量稀盐酸,观察到有气泡产生且_______,从而得出结论:步骤a中得到的白色沉淀全部是![]() ;
;
(3)丙同学取甲同学步骤b中已变红的溶液,向其中逐滴滴入稀硫酸,发现有白色沉淀生成且溶液褪色.根据有白色沉淀生成的现象确定原粉末中一定有________,一定没有________;溶液褪色的原因用化学方程式表示为_______。
(总结归纳)通过以上探究,原白色粉末中无法确定的成分是_______(填化学式)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液和氯化钡溶液五种溶液,为了鉴别和探究五种溶液,进行了下列相关实验,请回答
(1)根据溶液颜色即可确定硫酸铜溶液.取少量四种无色溶液分别放入四支试管中,再分别滴加硫酸铜溶液,出现白色沉淀的是氯化钡溶液;出现_____(填现象)的是_____(填溶液名称).
(2)另取少量剩余的两种溶液分别放入两支试管中,再分别滴加氯化钡溶液,其中一支试管内产生白色沉淀,该反应可用化学方程式表示为_____,至此,五瓶溶液已全部鉴别出来.
(3)氢氧化钠溶液露置在空气中易变质.下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是_____(填字母).
A 证明变质:取样,滴加足量稀盐酸,观察是否有气泡产生
B 除去杂质:取样,滴加氢氧化钙溶液至恰好完全反应,过滤
C 确定成分:取样,滴加足量氯化钡溶液,过滤,向滤液中滴加酚酞溶液,观察颜色变化(氯化钡溶液呈中性)
(4)当部分变质的氢氧化钠固体中,氢氧化钠和碳酸钠所含钠元素的质量相同时,该固体中氢氧化钠的质量分数为_____(计算结果精确到0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我区某校化学社团﹣﹣“拉瓦锡实验室”的同学们在化学实验室进行了一系列的实验探究活动.
(1)甲组同学的实验是除去粗盐中难溶性杂质,实验步骤主要有四步,如图1.
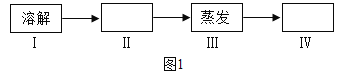
①步骤Ⅲ,给蒸发皿加热时_____(填“需要”或“不需要”)垫石棉网,当出现_____时,停止加热;
②步骤Ⅳ是_____.
(2)乙组同学进行的实验是“从NaCl和Na2CO3的混合物中提纯NaCl”.同学们经过讨论认为利用两物质化学性质的差异,可采用如下化学方法来提纯.
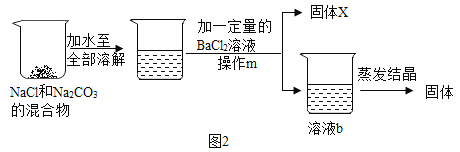
①如图2中X的化学式为_____.由于BaCl2溶液的用量不易控制,会使溶液b的溶质有多种情况,导致蒸发后得到的固体可能不纯.同学们对方案中溶液b的溶质成分进行了猜想.猜想一:NaCl、BaCl2 猜想二:NaCl 猜想三_____;
②经讨论,大家认为只用一种试剂就能判断出溶液b中溶质的成分,这种试剂是_____(写名称)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验操作,能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
B | 除去NaOH中混有的碳酸钠 | 滴加足量盐酸、蒸发 |
C | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入CuSO4溶液中 |
D | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、蒸发 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种含CaCO3与CaO的混合物,测得其中钙元素质量分数为50%.取该混合物16g,经高温煅烧后,将剩余固体投入足量水中,固体全部溶解生成Ca(OH)2,则生成的Ca(OH)2质量为( )
A.3.7gB.7.4gC.14.8gD.22.2g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组对“一氧化碳还原氧化铜”的实验进行拓展研究。
(查阅资料)
Ⅰ.制取 CO 的方法:加热碳酸镁和锌粉的混合物,反应原理为:MgCO3+Zn==MgO+ZnO+CO↑Ⅱ.处理尾气的方法:用氯化亚铜的氨水溶液吸收一氧化碳,溶液中会出现红色固体。
(设计方案)根据上述资料设计如下实验装置(固定装置略,装置气密性良好):
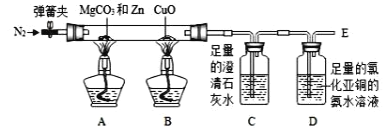
(实验步骤)
第一步:打开弹簧夹,通入一会儿氮气;
第二步:关闭弹簧夹,点燃两个酒精灯;
第三步:一段时间后,熄灭两个酒精灯;
第四步:……
(实验分析)
(1)实验过程中,观察到 B 处的实验现象是________;
(2)C 处发生反应的化学方程式是____________;
(3)D 处发生反应的化学方程式为:2CuCl+2CO+2X═Cu2Cl2(CO)2·2H2O↓,其中 X 的化学式为____________
(4)第四步操作是:打开弹簧夹,再通入氮气至____________。
(5)若 A 处有 mg MgCO3 参加反应,实验结束后 C 处生成 ng CaCO3,此时 D 装置的溶液中有红色固体析出,则 m 与 n 数量上的关系为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com