
【题目】(1)用化学用语表示:
① 2个氮分子_____ ② 3个硫酸根离子_____ ③ 碳酸钠____ ④氦气_______⑤ 氢氧化钙_____ ⑥ 地壳中含量最多的金属元素与含量最多的非金属元素形成的物质_________ ⑦保持二氧化碳化学性质的最小微粒_____
(2)写出下列符号的意义:
① 2H____________ ②4Fe2+___ ③![]() ____________
____________
【答案】2N2 3SO4 2- Na2CO3 He Ca(OH)2 Al2O3 CO2 2个氢原子 4个亚铁离子 五氧化二磷中,磷元素显+5价
【解析】
(1)①分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以2个氮分子可表示为2N2;②离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3个硫酸根离子可表示为:3SO42-;③碳酸钠是由显+1价的钠元素和显-2价的碳酸根组成,根据化合价原则,其化学式为:Na2CO3;④氦气是由氦原子直接构成的,其化学式为:He;⑤氢氧化钙是由显+2价的钙元素和显-1价的氢氧根组成,根据化合价原则,其化学式为:Ca(OH)2;⑥地壳中含量最多的金属元素是铝,含量最多的非金属元素是氧,据化合物化学式的书写规则,正负化合价的代数和为零,可知地壳中含量最多的金属元素与含量最多的非金属元素形成的物质是:Al2O3;⑦保持二氧化碳化学性质的最小微粒是二氧化碳分子,故化学式为:CO2;(2)①元素符号前面的数字表示原子的个数,故2H表示2个氢原子;②离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故4Fe2+表示4个亚铁离子;③元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以![]() 表示五氧化二磷中,磷元素显+5价。
表示五氧化二磷中,磷元素显+5价。


科目:初中化学 来源: 题型:
【题目】小明同学用下图总结了NaOH的化学性质(即NaOH与四类物质都能够发生化学反应)。

⑴反应③属于____________(填写基本反应类型)
⑵为了验证反应④能够发生,你选择的物质是___________。
A.Na2CO3 B.HCl C.CuSO4 D.NaCl
⑶依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述与对应的化学方程式、所属基本反应类型都正确的是( )
A. 氢气还原氧化铜 CuO+ H2![]() H2O + Cu 置换反应
H2O + Cu 置换反应
B. 加热煮沸降低水的(暂时)硬度 Ca(HCO3)2![]() CaCO3↓+ H2O+CO2↑ 分解反应
CaCO3↓+ H2O+CO2↑ 分解反应
C. 中和印染厂的废水 Ca(OH) 2+ H2SO4=CaSO4 +2H2O 复分解反应
D. 酸雨的pH<5.6 H2O + SO2=H2SO4 化合反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类和类比是学习化学常用的方法。
(1)按照影响化学实验的因素是一种还是多种,可将化学实验分为:研究单因素问题的实验;研究多因素问题的实验。据此应将下列实验中的A与①______(填字母)归为一类,依据是②___________________。

(2)盐可看作是酸、碱中和的产物,而由不同的酸碱生成的盐的水溶液不一定呈中性。强酸弱碱生成的盐水溶液呈酸性;弱酸强碱生成的盐水溶液呈碱性。强酸:盐酸、硫酸等;弱酸:碳酸、醋酸等;强碱:氢氧化钠、氢氧化钾等;弱碱:氨水、氢氧化铁等。碳酸钠溶液呈碱性是因为其在水中电离出的碳酸根离子水解,最终产生氢氧根离子。请据此推断硫铵水溶液的pH______(填“>”或 “<”)7;原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F、G都是初中化学中常见物质,A是白色固体,B和F是黑色固体,G和H是无色液体,E在D中燃烧的现象非常剧烈,火星四射。B在反应③中作催化剂。它们之间的转换关系如图所示:
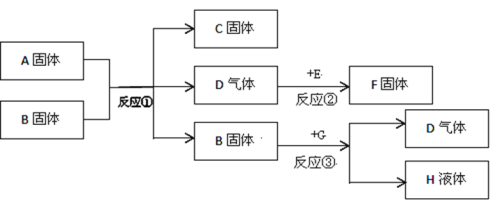
(1)写出上述物质的化学式:A________;G___________。
(2)写出上述①②③反应的化学方程式并在括号里注明该反应的基本反应类型。
①____________________ (____________)反应
②__________________________ (____________)反应
③____________________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验课上,同学们发现一瓶久置空气中的氧化钠固体的瓶口有白色粉末。在老师指导下,同学们对该白色粉末的成分进行了讨论。
(猜想与假设) 猜想I:白色粉末是碳酸钠
猜想II:白色粉末是氢氧化钠
猜想III:白色粉末是_____________________
(查阅资料)CaCl2溶液,Ca(NO3)2溶液呈中性。
(实验探究)取白色粉末溶于水形成溶液A,设计如下实验:
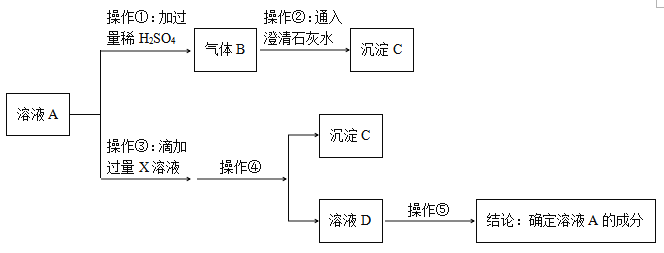
(1)由上述实验可知,猜想_______肯定不成立。
(2)若操作①滴加过量稀盐酸有气体B产生,而滴加少量稀硫酸可能没有气体B产生。其可能的原因是:_____________(用化学方程式回答)。
(3)适合操作③的X溶液是_______(填字母序号)。
A. CaCl2溶液 B. Ca(OH)2溶液 C. Ba(OH)2溶液 D. Ca(NO3)2溶液
(4)操作④需要用到的玻璃仪器是______________。
(5)请写出操作⑤的两种方案并得出结论。
方案一:________________________________________。
方案二:_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以黄铁矿为原料生产硫酸的工艺流程图如下,请回答下列问题。
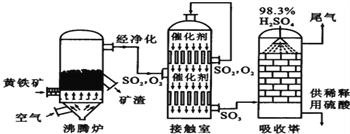
(1)在SO2、SO3、O2、H2SO4四种物质中属于氧化物的是___。
(2)在沸腾炉中发生反应的化学方程式为4___ +11O2=2Fe2O3+8SO2
(3)在接触室内化合价发生变化的元素是___。
(4)若有2000kg进入到吸收塔中,且完全被吸收,则所得的硫酸的质量是___。(已知:吸收塔内发生的化学反应是SO3+H2O=H2SO4)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学研究小组对蜡烛(主要由碳、氢元素组成)燃烧进行了如下探究。
(1)设计图 1 所示实验,锥形瓶中发生反应的化学方程式为_____; 请推测靠近三通管_____(填“上口”或“下口”)的火柴火焰熄灭,理由是_____________________。
(2)某同学用大烧杯将高低 2 支燃烧的蜡烛罩住(如图 2),观察到高的蜡烛先熄灭,低的 蜡烛后熄灭。

(提出问题)导致高的蜡烛先熄灭的原因是什么?
(猜想与假设)假设 1:可能是高蜡烛火焰附近的二氧化碳含量过大导致其先熄灭; 假设 2:可能是高蜡烛火焰附近的氧气浓度过低导致其先熄灭。
(设计实验)
甲同学按图 2 装置进行实验,点燃蜡烛,用大烧杯罩住。一段时间后,发现贴在烧杯内上部 的滤纸先褪色,说明此时高蜡烛附近的二氧化碳浓度比低蜡烛附近的浓度_____(填“高” 或“低”)。
(3)为进一步验证假设 1,乙同学收集 1 瓶含 20%氧气和 80%二氧化碳的气体,将点燃的蜡烛慢慢伸入瓶中并密封,蜡烛燃烧一段时间后慢慢熄灭,根据实验现象可知:假设 1_____(填“合理”或“不合理”)
(4)丙同学使用传感器测得密闭装置内蜡烛从燃烧到熄灭后的过程中(80s 时蜡烛熄灭), 装置内氧气和二氧化碳含量的变化曲线如图 3,则可得出蜡烛燃烧的条件是_________。
(5)结合已有知识和上述实验分析,乙同学实验中,蜡烛完全熄灭后瓶内含有的气体有_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com