
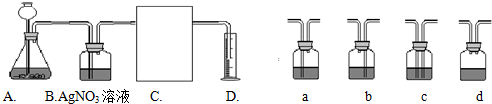


科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
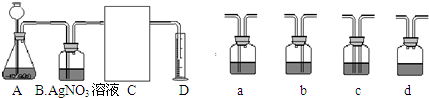
查看答案和解析>>
科目:初中化学 来源: 题型:
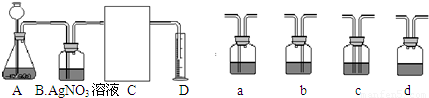
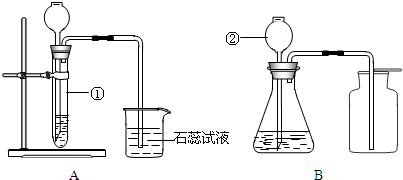 (2010?越秀区二模)某小组利用以下装置进行有关气体的实验室制法和性质的研究.
(2010?越秀区二模)某小组利用以下装置进行有关气体的实验室制法和性质的研究.查看答案和解析>>
科目:初中化学 来源:2012年广东省揭阳市揭东县地都四中中考化学模拟试卷(二)(解析版) 题型:解答题
 CO2
CO2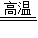 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑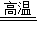 2Fe+3CO2
2Fe+3CO2| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com