
A、B、C是三种不同类别的含有氧元素的化合物,物质间相互反应的关系如图所示(图中“——”表示相连的两种物质能在溶液中发生反应)。若B 为纯碱,A、C间的反应为复分解反应。回答下列问题:
为纯碱,A、C间的反应为复分解反应。回答下列问题:

(1)物质A、C的化学式分别是 、 。
(2)物质A和C在溶液中反应的化学方程式是
。
(3)纯碱的一种用途是
。
 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源: 题型:
下列有关二氧化碳的说法错误的是
A.在空气中二氧化碳的体积分数约为0.03%
B.若二氧化碳在空气中含量过高,则会引发酸雨
C.过多的二氧化碳排放会导致温室效应
D.干冰可用于人 工降雨
工降雨
查看答案和解析>>
科目:初中化学 来源: 题型:
金属材料在国防建设中起着重要的作用,图1为歼﹣15飞机在航空母舰上起飞.
图1 图2
图2
(1)国防建设中大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如铝合金比纯铝的硬度 ▲ (填“大”或“小”).
(2)日常生活中铝制品比铁更耐腐蚀的原因是 ▲ (用化学方程式表示).
(3)钢铁的锈蚀主要是铁与空气中的 ▲ 、 ▲ 共同作用的结果.
(4)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属.小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是  ▲ .
▲ .
②实验二若出现 ▲ 现象,可证明铁的活动性强于铜.
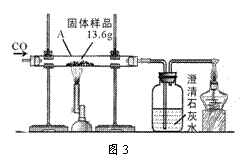
(5)某兴趣小组对一份含铁的固体样品进行探究.通过实验已确定该样品由氧化铁和铁粉混合而成.他们称取了13.6g固体样品,用图3所示的装置实验,测定的数据如图4所示.
①图3中硬质玻璃管中的生成铁的化学方程式为 ▲ .
②固体样品中氧化铁的质量是 ▲ 克.
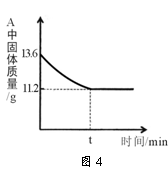 ③将上述反应后11.2g的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数 ▲ (结果精确到0.1%)(不写计算过程).
③将上述反应后11.2g的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数 ▲ (结果精确到0.1%)(不写计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:
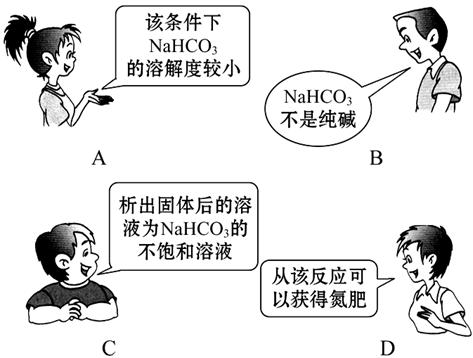
“NaCl+CO2+NH3+H2O====NaHCO3+NH4Cl”是著名的“侯氏制碱法”过程中的重要反应。下面是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是( )
查看答案和解析>>
科目:初中化学 来源: 题型:
分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是( )
A.NaNO3 NaCl H2SO4
B.CaCO3 NaOH Na2SO4
C.BaCl2 NaNO3 CuSO4
D.AgNO3 Na2SO4 NaCl
查看答案和解析>>
科目:初中化学 来源: 题型:
我市有丰富的石灰石资源,为了测定某地石灰石中碳酸钙的质量分数,取7.5g样品放入烧杯,加入稀盐酸至恰好不再产生气体时消耗34.7g,放出的气体在常温下体积为1.1L。
(1)常温下CO2气体的密度为2.0g/L,则上述反应放出气体的质量为 g。
(2)如石灰石中的杂质均不溶于水且不与盐酸反应,计算:
①石灰石中CaCO3的质量分数;
②反应所得溶液中溶质的质量分数(计算最终结果保留1位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
实验室有盐酸、白醋、柠檬酸三种溶液,回答下列问题:
(1)向三氧化二铁(红棕色固体)中放入足量盐酸,充分反应后,观察到的现象是 ,
反应的化学方程式是 。
(2)白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,说明白醋、柠檬酸溶液和盐酸中都含有的离子是 。
(3)理论上溶解3.2 g三氧化二铁,需要36.5%的盐酸多少克?(列式计算)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com