
��6�֣�H2��CO��CO2��CH4���dz��л�ѧ���������塣
1.��ȼ�������������ϵ�ȼ���ܻᱬը�����Կ�ȼ�������ȼǰӦ�� ��CH4��ȫȼ�յĻ�ѧ����ʽ�� ��
2.ij��ɫ����X���ܺ�������4�������е�һ�ֻ����֡�Ϊ��ȷ������X����ɣ�ͬѧ�ǰ���ͼװ�ý���ʵ�顣С���ϣ���ʯ�ҵ���Ҫ�ɷ���CaO��NaOH��
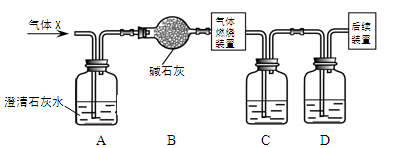
��ͬѧ�������װ��B���������� ��
��װ��C��D��ʢ�ŵ��Լ������� ������ţ���
a���ռ���Һ b��Ũ����
����ȡ1.6 g����X����ʵ�飨����ÿ����Ӧ����ȫ��������װ��A�������Ա仯��װ��C����1.8 g��װ��D����2.2 g��������X������� ��
��6�֣�
1.�鴿 CH4+ 2O2 CO2 + 2H2O
2.�ٳ�ȥCO2��H2O ��b a ��H2��CO����ȫ��2�֣�����0�֣�
����:
1.��ȼ�������������ϵ�ȼ���ܻᱬը�����Կ�ȼ�������ȼǰ������鴿�ȡ�2.�ټ�ʯ�ҵ���Ҫ�ɷ���CaO��NaOH�����Գ�ȥCO2��H2O ����Ҫ����Ũ������ˮ�������Ⱦ�������������Һ�����һ����ˮ������Ӱ��ʵ�飬��װ��C��D��ʢ�ŵ��Լ�������b a ����װ��A�������Ա仯˵��ԭ���������û�ж�����̼��װ��C����1.8 g˵������ˮ��1.8�ˣ�װ��D����2.2 g��˵�����ɶ�����̼2.2�ˣ������������������Ԫ������Ϊ0.2�ˣ�̼Ԫ������Ϊ0.6�ˣ���Ӧǰ��Ԫ���������䣬����1.6 g����X��Ҳ����0.2����Ԫ�غ�0.6��̼Ԫ�أ���ʣ���0.8��ӦΪ��Ԫ�أ�����X��һ������һ����̼����Ϊ������ˮ�����ݷ�Ӧ����������������ϵ������һ������������������������X�����ΪH2��CO��


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com