
 化学兴趣小组对铁的性质做了如下探究:
化学兴趣小组对铁的性质做了如下探究:分析 根据已有的金属的锈蚀因素的实验探究以及金属活动性的知识进行分析解答即可.
解答 解:(1)(1)①要知道铁锈蚀的因素,必须设计对比试验,因此甲同学认为,试管A发生的现象就能够说明铁的锈蚀是铁与空气中的氧气、水蒸气共同作用的结果的观点是不正确的,还需要观察试管BC,才能得出上述结论,故填:BC.
②探究铁在盐溶液中是否更容易锈蚀,则对比试管AD,故填:AD;
(2)由于金属铁是粉末,锌是粒状,与酸的接触面积不同,故这种方案不够合理,理由是金属与酸接触的面积不同,故填:金属与酸接触的面积不同;
(3)铁的活动性强于铜,弱与锌,故将过量的铁粉放入硝酸铜,硝酸锌的混合溶液中,铁与硝酸铜反应生成硝酸亚铁和铜,置换出的铜的质量大于生成的亚铁离子的质量,故充分反应后过滤,则反应后溶液质量比反应前减小,故填:减小.
点评 掌握金属的性质是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 自然界中的水中大多数为纯净物 | |
| B. | 农业上合理使用化肥和农药有利于水资源的保护 | |
| C. | 只有用蒸馏的方法才能降低水的硬度 | |
| D. | 我国可利用的淡水资源十分丰富 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Al3+-铝元素的化合价为+3 | |
| B. | 3H2O-3个水分子 | |
| C. | 3H-3个氢原子 | |
| D. | SO3-1个三氧化硫分子中含有3个氧原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 温度范围/℃ | 5~10 | 10~15 | 15~20 | 20~25 |
| 活性氧含量/% | 13.94 | 14.02 | 15.05 | 14.46 |
| “鱼浮灵”的产率/% | 85.49 | 85.78 | 88.38 | 83.01 |
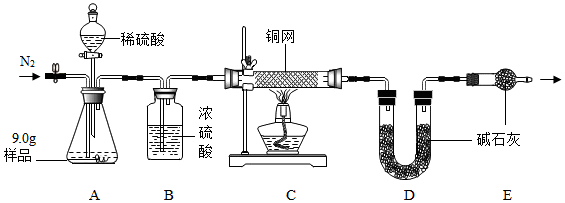
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
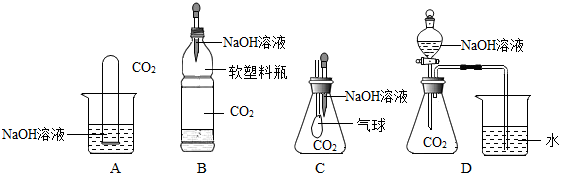
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
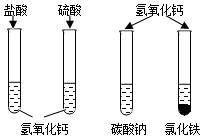
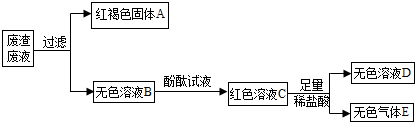
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com