
分析 20℃时氯化钠的溶解度为36g,其涵义是:20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态;据此判断20℃时将12、20克氯化钠放入到50克水中溶解的质量,进而计算出所得溶液的溶质的质量分数.
解答 解:20℃时氯化钠的溶解度为36g,其涵义是20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态,该温度下,将12g氯化钠放入50g水中,充分溶解,最多能溶解18g,充分搅拌后所得溶液的溶质的质量分数为$\frac{12g}{12g+50g}×$100%≈19.4%.
该温度下,若将20g氯化钠放入50g水中,充分溶解,最多只能溶解18g,形成的是饱和溶液,溶液的溶质质量分数为$\frac{18g}{18g+50g}$×100%≈26.5%.
故答案为:19.4%;26.5%;饱和.
点评 本题难度不大,理解溶解度的概念,熟练掌握溶质质量分数的有关计算是正确解答本题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
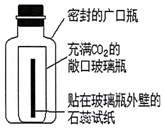 利用如图所示装置探究CO2能与水反应.
利用如图所示装置探究CO2能与水反应.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 “空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
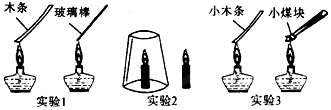
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
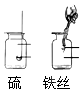 氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应.如图所示,关于这两个反应的叙述正确的是( )
氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应.如图所示,关于这两个反应的叙述正确的是( )| A. | 都发光发热 | B. | 生成物都是固体 | ||
| C. | 都产生蓝紫色火焰 | D. | 都是非金属和氧气反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4 | B. | Zn (OH)2 | C. | Na2O | D. | KOH |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
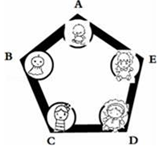 兴趣小组把A、B、C、D、E围成如图所示的“化学游乐城”,已知盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠是五种物质的选项,游娱规则为只有相邻物质间能发生反应才能组成守护防线(如图所示),其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分(提示:碳酸钡不溶于水)
兴趣小组把A、B、C、D、E围成如图所示的“化学游乐城”,已知盐酸、硫酸、氢氧化钠、氯化钡和碳酸钠是五种物质的选项,游娱规则为只有相邻物质间能发生反应才能组成守护防线(如图所示),其中物质A常用于铅酸蓄电池中,其浓溶液有脱水性;物质C是人体胃液中的主要成分(提示:碳酸钡不溶于水)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
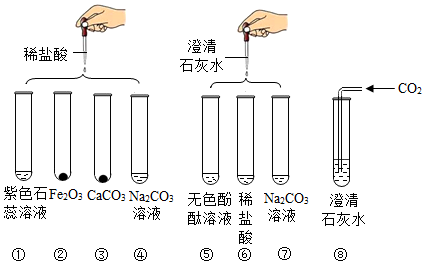
| 步骤 | 操作 | 现象 | 结论 |
| 第一步 | 取样,加入少量盐酸 | 无气泡产生 | 废液中一定没有碳酸钠 |
| 第二步 | 再次取样,进行实验⑧ | 无白色沉淀产生 | 废液中只有氢氧化钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com