
分析 根据已有的知识进行分析,钡离子与硫酸根离子结合生成的硫酸钡是不溶于酸的白色沉淀,氢氧根离子能与镁离子结合生成氢氧化镁白色沉淀,氢氧化镁是溶于酸的沉淀,据此解答即可.
解答 解:(1)①取一份废液,加入氯化钡溶液有白色沉淀产生,钡离子能与硫酸根离子结合产生硫酸钡白色沉淀,钡离子能与碳酸根离子结合产生碳酸钡白色沉淀,再加入足量稀盐酸,沉淀无变化,说明生成的是硫酸钡沉淀,不是碳酸钡沉淀,故废液中一定含有硫酸根离子,一定不含有碳酸根离子,由于有硫酸根离子,故一定不会含有钡离子;
②另取一份废液,加入氢氧化钾溶液出现白色沉淀,镁离子能与氢氧根离子结合生成溶于盐酸的氢氧化镁沉淀,故废液中一定含有镁离子;
通过分析可以知道,废液中可能含有氯离子和钾离子;
故溶液中一定含有Mg2+、SO42-,一定没有的离子是Ba2+、CO32-;可能含有Cl-、K+.
(2)取一份废液先滴加足量的硝酸钡溶液,将溶液中的硫酸根离子除掉,再过滤向滤液中滴加硝酸银溶液,如果有白色沉淀生成,说明含有氯离子.
答案:(1)Mg2+、SO42-;Ba2+、CO32-;Cl-、K+.
(2)取一份废液先滴加足量的硝酸钡溶液,再过滤向滤液中滴加硝酸银溶液;有白色沉淀生成.
点评 本题考查了常见离子的检验,完成此题,可以依据已有的关于离子的性质进行.要求同学们加强对离子性质的掌握,以便灵活应用.


 考前必练系列答案
考前必练系列答案科目:初中化学 来源: 题型:选择题
 ”和“
”和“ ”分别表示不同的原子.下列说法正确的是( )
”分别表示不同的原子.下列说法正确的是( )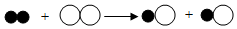
| A. | 反应前后分子的种类没有改变 | B. | 反应物和生成物中共含有三种元素 | ||
| C. | 参加反应的物质分子个数比为1:1 | D. | 反应物和生成物分别都是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
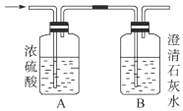 如图,某气体X可能由H2、CO、CH4中的一种或几种组成,将X气体点燃,把燃烧后生成的气体通过A、B两个洗气瓶.试完成下列问题:
如图,某气体X可能由H2、CO、CH4中的一种或几种组成,将X气体点燃,把燃烧后生成的气体通过A、B两个洗气瓶.试完成下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 回答下列问题:
回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
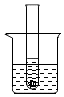 如图所示,在盛有冷水的烧杯中放着一支试管,试管中是饱和的氯化钠溶液和部分未溶的氯化钠固体.现向烧杯中的水中加入适量的氢氧化钠固体,再恢复到原来的温度,下列各相关的变化图象正确的是( )
如图所示,在盛有冷水的烧杯中放着一支试管,试管中是饱和的氯化钠溶液和部分未溶的氯化钠固体.现向烧杯中的水中加入适量的氢氧化钠固体,再恢复到原来的温度,下列各相关的变化图象正确的是( )| A. |  | B. | 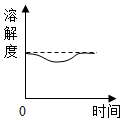 | C. |  | D. |  |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
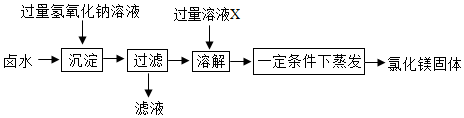
| 离子 | Cl- | Na+ | Mg2+ | Ca2+ | K+ | 其他 |
| 含量 | 55.06% | 30.61% | 3.69% | 1.15% | 1.10% | … |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com