
| 实验次数 | 1 | 2 | 3 | 4 |
| 每次加入样品的质量/g | 5 | 5 | 5 | 5 |
| 反应后剩余物质的总质量/g | 40.4 | 44.3 | m | 54.3 |
分析 氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据表中提供的数据可以进行相关方面的计算.
解答 解:(1)该实验产生了一种气体二氧化碳,二氧化碳的化学式为CO2;
由表格数据可知,第二次产生CO2的质量是36.5g+5g+5g-44.3g=2.2g,第四次产生二氧化碳的质量是:36.5g+5g+5g+5g+5g-54.3g=2.2g,故第三次产生二氧化碳的质量也是2.2g,故m的值为:36.5+5+5+5-2.2=49.3.
故填:CO2;49.3.
(2)由表格中数据分析可知,第二次进行的实验是恰好完全反应,即产生CO2的质量是36.5g+5g+5g-44.3g=2.2g时,氢氧化钠变质产生的碳酸钠完全反应,故设样品中变质产生碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$,
x=5.3g
烧碱样品中烧碱的纯度为:$\frac{10g-5.3g}{10g}$×100%=47%,
答:烧碱样品中烧碱的纯度为47%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:初中化学 来源: 题型:解答题
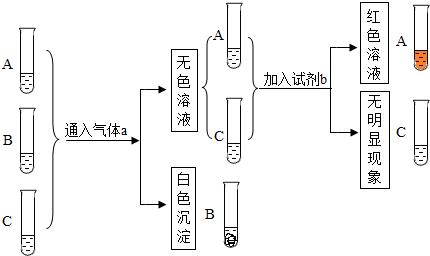
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
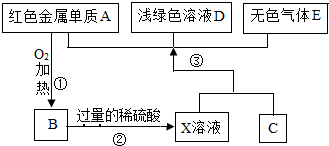 A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
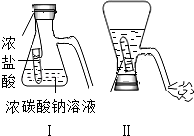 某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行探究.
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | O | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸根离子(或碳酸钠) | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com