
| A.硝酸铵 | B.氢氧化钙 | C.氯化钠 | D.氢氧化钠 |
科目:初中化学 来源: 题型:阅读理解
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量(g) | 43.6 | 待测数据 | 4.2 | 8.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 28、下表是某兴趣小组通过实验测得的A、B两种物质在各温度下的溶解度数值:
28、下表是某兴趣小组通过实验测得的A、B两种物质在各温度下的溶解度数值:| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| A物质的溶解度(g) | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| B物质的溶解度(g) | 27.6 | 31 | 34 | 37 | 40 | 42.6 | 45.5 | 48.1 | 51.1 | 54 | 56.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| NaHCO3 | Na2CO3 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
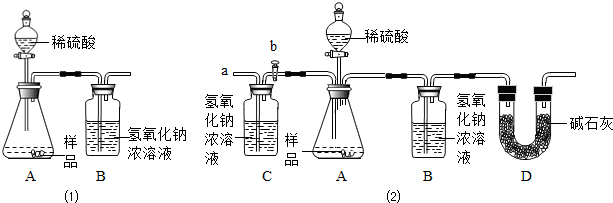
| 实验步骤 | 实验现象 | |
| ①取少量样品溶于水,加入过量的CaCl2溶液. | 有白色沉淀产生 有白色沉淀产生 ; |
该反应的方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl Na2CO3+CaCl2═CaCO3↓+2NaCl . |
| ②将上述反应后的混合液过滤,取滤液 滴加稀盐酸 滴加稀盐酸 . |
有气泡冒出 有气泡冒出 ; |
证明猜想②成立. |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (1)请你各举出一个实例,说明下列有关溶液的叙述是错误的.
(1)请你各举出一个实例,说明下列有关溶液的叙述是错误的.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com