
| A. | 水是由氢气和氧气组成的 | |
| B. | 正极上产生的气体与负极上产生的气体的质量比是1:2 | |
| C. | 电解水的实验可以证明原子是化学变化中的最小粒子 | |
| D. | 在电解水的实验中,每2份水分解可以生成2份氧气和1份氢气 |
分析 运用电解水的实验现象、结论进行分析:正极产生的是氧气;负极产生的是氢气,且正负极气体体积比为1:2;根据微粒的变化,分析分子、原子的变化.通过水电解的实验可以说明水由氢、氧两种元素组成的纯净物.
解答 解:A、电解水实验证明了水是由氢、氧元素组成的一种化合物,故A错误;
B、正极上产生的气体与负极上产生的气体的体积比是1:2,而不是质量比,故B错误;
C、电解水的实验中原子的种类和数目不变,所以可以证明原子是化学变化中的最小粒子,故C正确;
D、在电解水的实验中,每26份水分解可以生成32份氧气和4份氢气,故D错误.
故选C.
点评 通过电解水的实验,可以证明水由H、O元素组成,根据电解生成氢气、氧气体积比2:1,可推导水分子中氢、氧原子个数比为2:1.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 黄金与黄铜(铜锌合金)-灼烧 | B. | 氯化钾与氯化铵-用熟石灰 | ||
| C. | 氧气与氮气-闻气味 | D. | 蒸馏水与氯化镁溶液-肥皂水鉴别 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
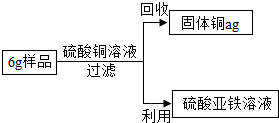 兴趣小组的同学为测定某一铁铜合金中含铁的质量分数,将6g该合金粉末样品,加入溶质质量分数为10%的硫酸铜溶液160g中,二者恰好完全反应.同时为了充分利用资源,还对反应后的物质进行回收处理.请结合下面图示计算.(计算结果均保留小数点后一位有效数字)
兴趣小组的同学为测定某一铁铜合金中含铁的质量分数,将6g该合金粉末样品,加入溶质质量分数为10%的硫酸铜溶液160g中,二者恰好完全反应.同时为了充分利用资源,还对反应后的物质进行回收处理.请结合下面图示计算.(计算结果均保留小数点后一位有效数字)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
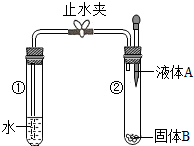 如图所示,打开止水夹,将液体A滴入试管②中与固体B接触.若试管①中的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )
如图所示,打开止水夹,将液体A滴入试管②中与固体B接触.若试管①中的导管口有较多气泡产生,则液体A和固体B的组合不可能是( )| A. | 水和硝酸铵 | B. | 水和生石灰 | ||
| C. | 水和氢氧化钠 | D. | 双氧水和二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
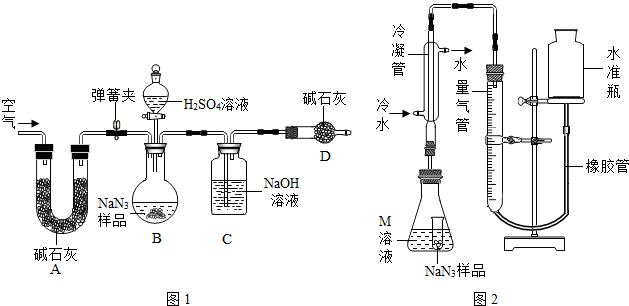
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com