
 有一包固体粉末,可能由BaSO4、CuSO4、Na2CO3、BaCl2、NaCl中的一种或几种组成,其实验小组对其成分进行了以下探究活动
有一包固体粉末,可能由BaSO4、CuSO4、Na2CO3、BaCl2、NaCl中的一种或几种组成,其实验小组对其成分进行了以下探究活动分析 (1)根据常见盐的溶解性,进行分析解答.
(2)根据溶解操作所需的仪器,进行分析解答.
(3)根据碳酸钠能与稀盐酸反应生成二氧化碳气体,Na2CO3、BaCl2不能共存,进行分析解答.
(4)根据盐的化学性质,进行分析解答.
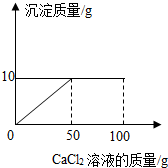
(5)碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,根据产生沉淀的质量与所加CaCl2溶液的质量关系图,当所加CaCl2溶液的质量为50g时,恰好完全反应,生成10g沉淀,由反应的化学方程式列式计算出样品中Na2CO3的质量、反应后所得溶液中CaCl2的溶质质量分数.
解答 解:(1)BaSO4、CuSO4、Na2CO3、BaCl2、NaCl中BaSO4不溶于水,硫酸铜溶于水其水溶液呈蓝色.
(2)取上述固体,加入足量水溶解,形成无色透明的溶液,则一定不含硫酸钡、CuSO4,Na2CO3、BaCl2在溶液中反应生成碳酸钡白色沉淀,则Na2CO3、BaCl2不能共存.在溶解过程中要用到的玻璃仪器有烧杯和玻璃棒.
(3)再向上述溶液中加入盐酸,产生大量的气泡,碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳气体,则说明该固体中一定含有Na2CO3,一定不含氯化钡;反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(4)氯化钠与上述物质均不反应,经过以上探究,不能确定的物质是氯化钠.
(5)①由图示可知,恰好完全反应时生成沉淀的质量是10g.
②设样品中Na2CO3的质量为x,参加反应的氯化钙的质量为y,
CaCl2+Na2CO3═CaCO3↓+2NaCl
111 106 100
y x 10g
$\frac{106}{100}=\frac{x}{10g}$ x=10.6g
③$\frac{111}{100}=\frac{y}{10g}$ y=11.1g
由图示可知,恰好完全反应后剩余的溶液中还氯化钙的质量也为11.1g.
反应后所得溶液中CaCl2的溶质质量分数是$\frac{11.1g}{22g+110g+100g-10g}$×100%=5%.
故答案为:(1)BaSO4;CuSO4;(2)烧杯;玻璃棒;(3)Na2CO3,Na2CO3+2HCl═2NaCl+H2O+CO2↑;(4)NaCl;(5)①10g;②22克样品中Na2CO3的质量是10.6g;③反应后所得溶液中CaCl2的溶质质量分数是5%.
点评 本题有一定难度,熟练掌握盐的化学性质、常见盐的溶解性、化学方程式与溶质质量分数的综合计算是正确解答本题的关键.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:初中化学 来源: 题型:推断题
 化学活动小组同学利用一些初中常见化学物质完成了制取某化工产品G的实验,同时还验证了相关物质的化学性质,其实验流程如图所示(反应条件已略去).其中A是一种常见的建筑材料,G被广泛用于肥皂、造纸、纺织、印染等工业,请回答如下问题:
化学活动小组同学利用一些初中常见化学物质完成了制取某化工产品G的实验,同时还验证了相关物质的化学性质,其实验流程如图所示(反应条件已略去).其中A是一种常见的建筑材料,G被广泛用于肥皂、造纸、纺织、印染等工业,请回答如下问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石块粉碎 | B. | 扎实路基 | C. | 铁轨氧焊 | D. | 灯泡发光 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
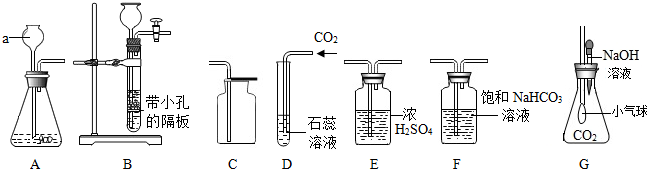
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KNO3是复合肥料 | |
| B. | 残留农药可通过农作物转移到人体中 | |
| C. | 熟石灰可用于改良酸性土壤 | |
| D. | 化肥能提高粮食产量,施用越多越好 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
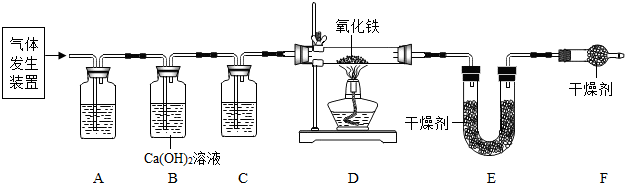
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
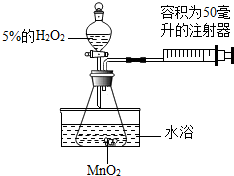 小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:
小金为了探究温度对H2O2分解反应速率的影响,借助如图所示实验装置(夹持装置略去),进行了两次实验,两次实验的部分设计如表所示:| 实验1 | 实验2 | |
| MnO2的质量/克 | 0.5 | 0.5 |
| 5%的H2O2的体积/毫升 | 40 | 待填 |
| 水浴温度/℃ | 20 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在硝酸铵溶液中:Na+、Cu2+、OH- | B. | 在稀盐酸中:Ba2+、CO32-、Zn2+ | ||
| C. | 在氯化钠溶液中:K+、Ca2+、NO3- | D. | 在氢氧化钠溶液中:H+、Mg2+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com