
(4分) 某气体X可能是由H2、CO、CO2中的一种或两种组成,为了解其组成情况,某同学设计了如下装置进行实验 (假设各步反应均完全)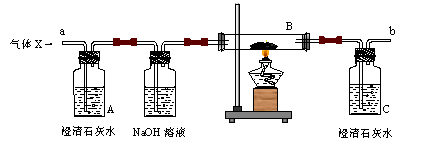
(1)请根据下表中对可能出现的实验现象的描述,推测气体X的组成情况,
| | 可能出现的实验现象 | 气体X的组成 | ||
| A中液体 | B中黑色粉末 | C中液体 | ||
| ① | 不浑浊 | 变成光亮的红色 | 不浑浊 | H2 |
| ② | 不浑浊 | 变成光亮的红色 | 变浑浊 | 一定有CO, 可能有H2 |
| ③ | 变浑浊 | 变成光亮的红色 | 不浑浊 | |
| ④ | 变浑浊 | 变成光亮的红色 | 变浑浊 | |
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 40.0 | 4.6 | 37.8 | 0.0 |
| 反应后质量(g) | 43.6 | 待测数据 | 4.2 | 8.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源:2011届江苏省苏州市草桥中学九年级上学期期中考试化学试卷(带解析) 题型:探究题
(4分)载人航天工程有许多问题需要解决,舱内气体净化就是其中之一。某化学兴趣小组准备探究二氧化碳转化成氧气的方法。
【查阅资料】
超氧化钾固体(化学式KO2)可作氧气源,用于呼吸面罩,供水下、矿井、高山、高空作业时使用。利用它能与二氧化碳反应放出氧气的原理,可作为密闭系统(如潜艇、宇宙太空舱等)的氧气再生剂。
【提出问题】
超氧化钾与二氧化碳反应除了生成氧气以外,还生成什么?
【猜想与假设】(1)根据化学反应前后元素种类不变,超氧化钾与二氧化碳反应的产物是氧气和化合物X,X中一定含 元素。
【实验验证】
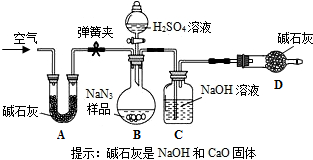
(2)兴趣小组同学设法排尽A中的原有空气后依次连接装置A、B、C进行实验(仪器b为U型管,超氧化钾)。装置A的作用是 ;
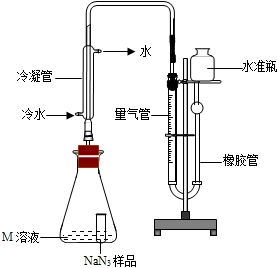
按装置A,B,C依次连接,在C装置的后面连接一个量筒,收集氧气所排出的水,可以粗略测量氧气体积,但小敏经过多次实验发现,利用该装置测得生成氧气体积偏大的最主要原因是 。
(3)小米同学在B装置和C装置之间连接一个与装置C相同洗气瓶,瓶中放半瓶澄清石灰水,反应刚开始瓶中出现很多气泡但石灰水几乎没有浑浊,但是过了一段时间后,石灰水出现较大量的浑浊,这现象说明什么 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com