
| A. | 1000g | B. | 1110g | C. | 543.5mL | D. | 1840mL |
分析 根据98%的浓H2SO4中硫酸和水的物质的量之比是:$\frac{98g}{98g/mol}$:$\frac{2g}{18g/mol}$=1:$\frac{1}{9}$,所以98%的浓硫酸可以表示为:SO3•$\frac{10}{9}$H2O,吸收三氧化硫后,得到纯H2S2O7,可以表示为:2SO3•H2O,进一步表示为:$\frac{20}{9}$SO3•$\frac{10}{9}$H2O,计算浓硫酸改写后水的物质的量,可得$\frac{20}{9}$SO3•$\frac{10}{9}$H2O的物质的量,再利用硫原子守恒计算H2SO4•$\frac{1}{9}$H2O的物质的量,进而计算质量.
解答 解:98%的浓H2SO4中硫酸和水的物质的量之比是:$\frac{98g}{98g/mol}$:$\frac{2g}{18g/mol}$=1:$\frac{1}{9}$,所以98%的浓硫酸可以表示为:SO3•$\frac{10}{9}$H2O,吸收三氧化硫后,得到纯H2S2O7,可以表示为:2SO3•H2O,进一步表示为:$\frac{20}{9}$SO3•$\frac{10}{9}$H2O,浓硫酸改写后水的物质的量:n(H2O)=500g÷(80+$\frac{10}{9}$×18)×$\frac{10}{9}$=$\frac{50}{9}$mol,则$\frac{20}{9}$SO3•$\frac{10}{9}$H2O的物质的量为:10mol,根据硫原子守恒,可得浓硫酸H2SO4•$\frac{1}{9}$H2O物质的量为:$\frac{100}{9}$mol,所以浓硫酸质量为:$\frac{100}{9}$mol×(98+2)g/mol=1110g.
故选:B.
点评 本题主要考查了溶液浓度的计算,难度较大,注意元素守恒以及物质的量的应用.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | CH4•H2O晶体中水是溶剂 | B. | CH4•H2O的组成元素有三种 | ||
| C. | 可燃冰是一种纯净物 | D. | 可燃冰燃烧说明水具有可燃性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
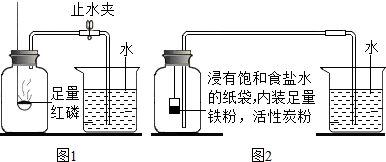
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 ,该原子在化学反应易失去(填“得到”或“失去”)电子,说明元素的化学性质与原子的最外层电子数关系密切.
,该原子在化学反应易失去(填“得到”或“失去”)电子,说明元素的化学性质与原子的最外层电子数关系密切.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在生活与学习中,一些青少年学生由于长时间玩手机、用电脑或看书写字姿势不科学等行为,很容易造成眼睛近视,就会配戴类似如图所示的近视眼镜.
在生活与学习中,一些青少年学生由于长时间玩手机、用电脑或看书写字姿势不科学等行为,很容易造成眼睛近视,就会配戴类似如图所示的近视眼镜.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com