
分析 (1)根据碳酸钙和稀盐酸反应的现象进行分析;
(2)根据化学反应的方程式,计算出生成气体的质量,依据质量守恒定律即可求得烧杯中溶液的质量.
解答 解:(1)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,所以观察到的明显实验现象是:固体逐渐溶解,有气泡冒出;
(2)加入盐酸的质量为:10%×73g=7.3g,
设生成CO2的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
73 44
7.3g x
$\frac{73}{44}=\frac{7.3g}{x}$ 解得 x=4.4g
所以烧杯中所得溶液的质量为:178g+22g+73g-4.4g=268.6g.
故答案为:(1)固体不断溶解,有气体产生;(2)268.6g.
点评 溶液和化学反应融合的题目,是综合性的题型,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,这就要求学生足够细心、会分析、且条理分明.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 (1)向一盛有少量干冰的玻璃容器中加入适量热水,立即产生浓厚的白雾,产生此现象的原因是干冰升华吸热,使周围的水蒸气冷凝成小水珠.
(1)向一盛有少量干冰的玻璃容器中加入适量热水,立即产生浓厚的白雾,产生此现象的原因是干冰升华吸热,使周围的水蒸气冷凝成小水珠.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
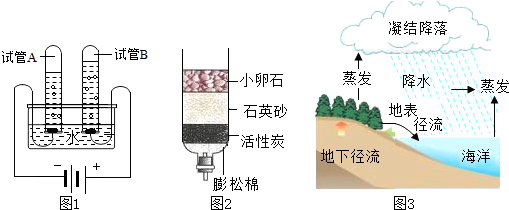
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
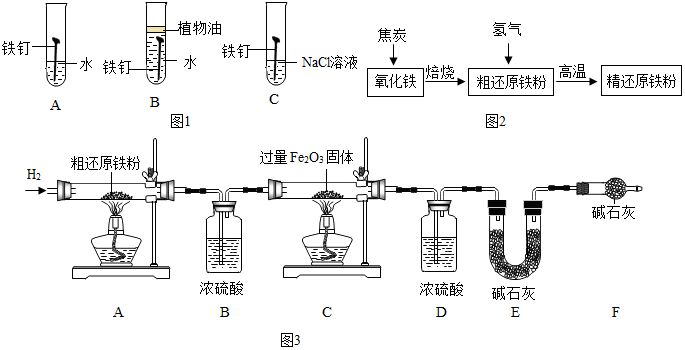
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用漱口杯接水刷牙 | |
| B. | 不间断地边流水边洗衣 | |
| C. | 用淘米水、洗菜水浇花、冲厕所 | |
| D. | 用喷灌、滴灌的方法浇灌农田和园林 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
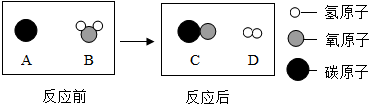
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com