
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中铁元素的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
[资料1]碱石灰既能吸收水又能吸收二氧化碳;浓硫酸可以吸收水蒸气;
[资料2]实验室常用氢氧化钠溶液来除去CO2 反应生成碳酸钠和水;用澄清的石灰水
来检验CO2气体;
[资料3]草酸晶体(H2C2O43H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O43H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
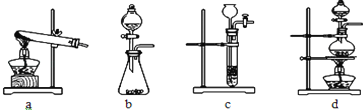
(1)下列可用作草酸分解制取气体的装置是 (填字母编号).
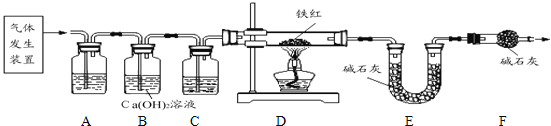
【问题讨论】用下图所示装置进行实验:
(2)实验前应先 .
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是 、 (填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)写出A装置中发生的化学反应方程式 .
(5)B装置的作用是 .
(6)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前 . ②停止加热后 .
(7)写出D装置中所发生反应的一个化学方程式 .
【数据分析与计算】
[资料4]铁的常见氧化物中铁的质量分数:
铁的氧化物 FeO Fe2O3 Fe3O4
铁的质量分数 77.8% 70.0% 72.4%
(8)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则 <m< .
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是 .
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会 (填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷 .
【答案】(1)d(2)检查装置的气密性.
(3)c;a(4)CO2+2NaOH=Na2CO3+H2O.
(5)验证CO2已除尽.
(6)将装置中的空气排出,防止发生爆炸;驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收,同时能够防止空气进入,铁被氧化.
(7)Fe2O3+3CO![]() 2Fe+3CO2.
2Fe+3CO2.
(8)①7.0;7.78②76.0%.
【实验评价】偏小;
【问题讨论】缺少尾气处理装置,或没有检验水是否除尽.
【解析】(1)草酸晶体(H2C2O43H2O)在浓硫酸作用下受热分解生成一氧化碳等物质,因此应该用d装置作为发生装置.
(2)实验前应先检查装置的气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是氢氧化钠溶液、浓硫酸.
(4)A装置中,二氧化碳和氢氧化钠反应生成碳酸钠和水,发生的化学反应方程式为:CO2+2NaOH=Na2CO3+H2O.
(5)B装置的作用是验证CO2已除尽.
(6)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前,将装置中的空气排出,防止发生爆炸;
②停止加热后,驱赶装置中滞留的二氧化碳,使其全部被E装置中碱石灰全部吸收,同时能够防止空气进入,铁被氧化.
(7)D装置中,氧化铁和一氧化碳反应生成铁和二氧化碳,氧化亚铁和一氧化碳反应生成铁和二氧化碳,四氧化三铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式分别是:Fe2O3+3CO![]() 2Fe+3CO2,FeO+CO
2Fe+3CO2,FeO+CO![]() Fe+CO2,Fe3O4+4CO
Fe+CO2,Fe3O4+4CO![]() 3Fe+4CO2.
3Fe+4CO2.
(8)①如果全部是氧化铁,铁的最少量是10g×70%=7.0g,如果全部是氧化亚铁,铁的最大量是10g×77.8%=7.78g.
②由Fe2O3+3CO![]() 2Fe+3CO2,FeO+CO
2Fe+3CO2,FeO+CO![]() Fe+CO2,Fe3O4+4CO
Fe+CO2,Fe3O4+4CO![]() 3Fe+4CO2可知,二氧化碳中的氧元素质量一半来自于一氧化碳,一半来自于铁的氧化物,E装置增重6.6g,说明生成二氧化碳的质量是6.6g,6.6g二氧化碳中氧元素的质量为:6.6g×3244×100%=4.8g,那么铁的氧化物中氧元素的质量是4.8g÷2=2.4g,
3Fe+4CO2可知,二氧化碳中的氧元素质量一半来自于一氧化碳,一半来自于铁的氧化物,E装置增重6.6g,说明生成二氧化碳的质量是6.6g,6.6g二氧化碳中氧元素的质量为:6.6g×3244×100%=4.8g,那么铁的氧化物中氧元素的质量是4.8g÷2=2.4g,
则铁红中铁的质量分数=10g﹣2.4g10g×100%=76.0%,
【实验评价】
本实验中如果缺少C装置(不考虑其它因素),水蒸气会进入E装置中,从而导致二氧化碳的质量偏大,铁的氧化物中氧元素质量偏大,铁元素质量偏小,导致测得样品中铁的质量分数会偏小;
【问题讨论】中实验装置的明显缺陷是缺少尾气处理装置,没有检验水是否除尽.
故填:缺少尾气处理装置,或没有检验水是否除尽.


科目:初中化学 来源: 题型:
【题目】普通锌锰电池由锌、碳棒和黑色糊状五物组成,其中黑色糊状物的主要成分是淀粉、氯化铵、氯化锌和二氧化锰等。某研究性学习小组设计如下流程,变废为宝。

(1)“溶解”操作中,为提高溶解速率,可采取的措施是 等;“操作I”的名称是 ,请写出实验室进行该操作用到的一种仪器名称 。
(2)废旧干电池处理后得到的碳棒,具有导电性,还有 等(填一种即可)化学性质,请写出具有这种性质的一个反应化学方程式
(3)黑色滤渣中的二氧化锰与浓盐酸共热反应可制氯气(Cl2),同时生成氯化锰(MnCl2)和一种氧化物,该反应的化学方程式是
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是一种重要的资源。

(1)电解水实验揭示了水的组成。右图实验中得到氢气的试管是 (填“1”或“2”)。反应的化学方程式为 。
(2)自来水厂净水过程中用到活性炭,其主要作用是 。
(3)水变成水蒸气的过程中,不发生变化的是 (填字母序号)。
A.物质种类 B.分子质量 C.分子种类 D.分子间隔
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源是人类活动的物质基础,清洁能源、可再生能源具有广阔的开发与应用前景。
(1)化石燃料为不可再生能源,包括_____、石油和天然气。
(2)北京市部分公交柴油车更换为CNG(压缩天然气)燃料车。改用CNG作为公交车燃料的优点是_____(答一条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】84消毒液是一种有刺激性气味的高效液体消毒剂.主要成分为次氯酸钠(NaClO),广泛用于宾馆、旅游、医院、食品加工、家庭等的卫生消毒.请阅读信息并回答:

(1)次氯酸钠的制取原理是氯气与氢氧化钠反应生成氯化钠,次氯酸钠和水,化学反应方程式为 ;
(2)消毒液中次氯酸钠自身没有消毒作用,有消毒作用的是次氯酸钠与空气中二氧化碳反应得到的次氯酸(HClO),化学方程式为 .
(3)84消毒液是含氯消毒剂,氯气是一种挥发性的有毒气体,因此,84消毒液必须 保存.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)用下列物质的序号填空:
①石灰石 ②氢氧化钠 ③氧化钙 ④一氧化碳 ⑤熟石灰 ⑥稀盐酸
常用作食品干燥剂的是 ;常用建筑材料的是 ;
可用于改良酸性土壤的是 ;可用于金属表面除锈的是 ;
有毒的气体的是 ;
用于肥皂、石油、造纸、纺织、印染等工业的碱是 .
(2)硒被誉为“抗癌大王”.根据如图提供的有关硒的信息填空:

硒(Se)属于 (填“金属”或“非金属”)元素,其相对原子质量为 ,在化学反应中,硒原子容易 (填“得到”或“失去”)电子形成硒离子 (写离子符号).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】地震发生后,搜救犬能根据人体发出的气味发现幸存者。从微观的角度分析搜救犬能发现幸存者的原因是
A.分子的质量很小 B.不同分子性质不同
C.分子在不断运动 D.分子间有间隔
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】元素周期表是学习和研究化学的重要工具.回答下列问题:
(1)元素周期表中不同元素间最本质的区别是 (填字母).
A.质子数不同 B.中子数不同 C.相对原子质量不同
(2)1869年, (填字母)发现了元素周期律并编制出元素周期表.
A.张青莲 B.门捷列夫 C.拉瓦锡
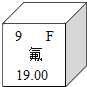
(3)元素周期表中氟元素的有关信息如图所示,下列说法正确的是 (填字母).
A.氟属于金属元素 B.氟的原子序数是9 C.氟的相对原子质量是19.00g
(4)氟原子结构示意图为![]() ,氟原子在化学反应中易 (填“得到”或“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为 .
,氟原子在化学反应中易 (填“得到”或“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com