
| 装置 | 反应前装置的质量/g | 反应后装置的质量/g |
| B | M | N |
| C | m | n |
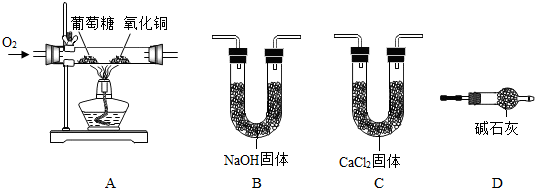
分析 (1)通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成,先吸收水,后吸收二氧化碳;
(2)C装置的质量增加是水的质量;
(3)装置D是为了防止空气中的二氧化碳和水分被装置C吸收测定结果偏高.
解答 解:(1)通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成,由于NaOH固体既能吸收水,又能吸收二氧化碳,所以先用CaCl2固体吸收水,后用NaOH固体吸收二氧化碳,
(2)C装置的质量增加是水的质量,所以反应中生成水的质量是n-m;
(3)若实验不连接装置D,空气中的二氧化碳和水分被装置C吸收测定结果偏高.
故答案为:(1)CB
(2)n-m
(3)装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
点评 本题是一道综合实验题,主要考查学生运用所学化学知识综合分析和解决实际问题的能力.要结合各种装置的作用和物质的性质进行分析思考.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:初中化学 来源: 题型:填空题
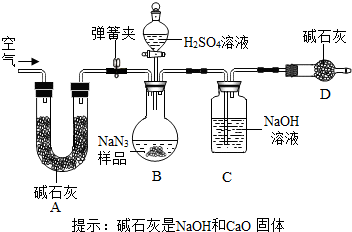 叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究.
叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某兴趣小组对其进行下列研究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用显微镜观察细胞时,先调节细准焦螺旋,后调节粗准焦螺旋 | |
| B. | 稀释浓硫酸时先将浓硫酸倒入烧杯中,后将水沿着烧杯壁慢慢倒入浓硫酸中 | |
| C. | 用氢气还原氧化铜时,应先通氢气一会儿,后点燃酒精灯加热 | |
| D. | 实验室制取氧气,停止加热时,应先熄灭酒精灯,再把导管移出水面 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe | B. | H2SO4 | C. | H2 | D. | FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 每年的3月22日是“世界水日”,水与人类生活和生产关系十分密切.根据所学知识回答下列问题.
每年的3月22日是“世界水日”,水与人类生活和生产关系十分密切.根据所学知识回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
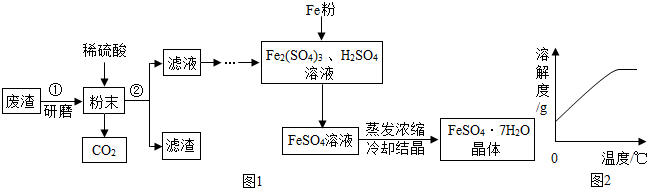
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 误服碳酸钡后用硫酸镁解毒:BaCl2+MgSO4═MgCl2+BaSO4↓ 复分解反应 | |
| B. | 石灰水刷墙,墙壁变白变硬:Ca(OH)2+CO2═CaCO3↓+H2O 非基本反应类型 | |
| C. | 向生石灰中加入石蕊溶液石灰水变蓝:CaO+H2O═Ca(OH)2 化合反应 | |
| D. | 在高炉中用赤铁矿炼铁:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com