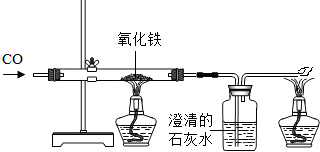
解:(1)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.
(2)为了防止钢铁的锈蚀,人们常采用在其表面刷油漆或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水.
(3)家庭厨房用完的菜刀要擦干存放,目的是除去水,防止生锈.
(4)铝在常温下与空气中的氧气反应,使其表面生成一层致密的氧化铝薄膜,阻止内部的铝进一步被氧化.
(5)二氧化碳和碳在高温条件下反应能生成一氧化碳,反应的化学方程式为:O
2+C

CO
2;
CO具有还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe
2O
3+3CO

2Fe+3CO
2.
(6)50%以上的废钢铁得到了回收利用,其目的是节约金属资源.
(7)解:设反应生成氢气的质量为X,
Zn+H
2SO
4═ZnSO
4+H
2↑
65 2
13g X
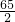
=

X=0.4g
故答案为:(1)氧气;水;(2)隔绝氧气; (3)除去水,防止生锈;(4)铝在常温下与空气中的氧气反应,使其表面生成一层致密的氧化铝薄膜,阻止内部的铝进一步被氧化;(5)①C+O
2 
CO
2;②3CO+Fe
2O
3 
2Fe+3CO
2;(6)节约金属资源;(7)答:可以生成氢气0.4g.
分析:(1)根据铁锈蚀的条件进行分析解答.
(2)铁与水、氧气充分接触时容易生锈,使铁制品与氧气和水隔绝可以防止生锈.
(3)根据防止铁锈蚀的措施进行分析解答.
(4)根据铝的化学性质进行分析.
(5)碳在高温条件下与氧气反应能生成二氧化碳,一氧化碳和氧化铁在高温条件下反应能生成铁和二氧化碳,写出反应的化学方程式即可.
(6)根据废钢铁回收利用的意义进行分析判断.
(7)根据化学方程式计算的一般步骤计算即可解决.
点评:本题考查了与铁有关的知识,明确铁的生锈及防锈,铝的化学性质以及高炉炼铁的原理和根据化学方程式的计算步骤是解答本题关键,难度不大.

 CO2;
CO2; 2Fe+3CO2.
2Fe+3CO2.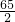 =
=
 CO2;②3CO+Fe2O3
CO2;②3CO+Fe2O3  2Fe+3CO2;(6)节约金属资源;(7)答:可以生成氢气0.4g.
2Fe+3CO2;(6)节约金属资源;(7)答:可以生成氢气0.4g.

 名校课堂系列答案
名校课堂系列答案
 钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.
钢铁是重要的金属材料,在建造淮安涟水飞机场时就是用了大量的钢铁.