
| 反应时间 | t1 | t2 | t3 | t4 | t5 |
| 试管内剩余固体质量/g | 31.6 | 31.0 | 29.6 | 28.8 | 28.8 |
分析 高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,由表格数据分析可知,最终试管内剩余固体的质量为28.8g,由质量守恒定律,固体混合物减少的质量即为生成氧气的质量,由反应的化学方程式列式计算出参加反应的高锰酸钾的质量,进而计算出样品中高锰酸钾的质量分数、剩余固体中锰元素的质量分数.
解答 解:(1)由质量守恒定律,生成氧气的质量为32g-28.8g=3.2g.
设参加反应的高锰酸钾的质量为x,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{32}=\frac{x}{3.2g}$ x=31.6g
样品中高锰酸钾的质量分数为$\frac{31.6g}{32g}$×100%=98.75%.
(2)由质量守恒定律,反应前后锰元素的质量不变,则高锰酸钾中锰元素的质量即为剩余固体中锰元素的质量,即31.6g×$\frac{55}{39+55+16×4}×$100%=11g.
剩余固体中锰元素的质量分数为$\frac{11g}{28.8g}$×100%≈38.2%.
答:(1)样品中高锰酸钾的质量分数为98.75%;
(2)剩余固体中锰元素的质量分数为38.2%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:选择题
| A. | CuSO4 HCl NaOH | B. | KOH HCl NaCl | ||
| C. | H2SO4 CuSO4 HCl | D. | KOH MgSO4 KNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳酸氢铵要保存在阴凉干燥处 | B. | 60℃以上碳酸氢铵会发生分解反应 | ||
| C. | 烤制后的饼干中还有碳酸氢铵 | D. | 使用碳酸氢铵可使糕点更加松软 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 黄铜是铜、锌合金,它用于制造机器、电器零件等.为测定某黄铜样品中铜的质量分数,取20g该黄铜样品加入到100g稀硫酸中,恰好完全反应.如图为反应产生的氢气质量与时间的关系图.
黄铜是铜、锌合金,它用于制造机器、电器零件等.为测定某黄铜样品中铜的质量分数,取20g该黄铜样品加入到100g稀硫酸中,恰好完全反应.如图为反应产生的氢气质量与时间的关系图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
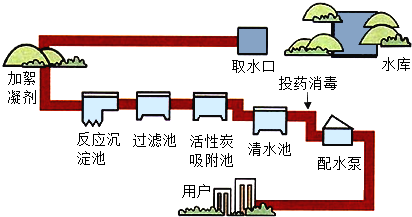 人类的生活和工农业生产都离不开水,如图是自来水厂净水过程示意图.
人类的生活和工农业生产都离不开水,如图是自来水厂净水过程示意图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
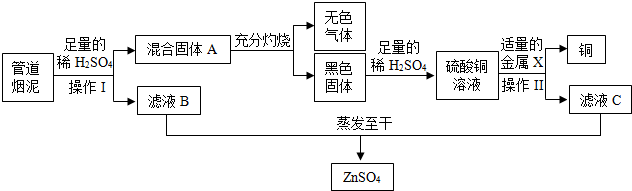
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 区别方法 | |
| A | 硬铝和铝 | 相互刻画 |
| B | 氢气和甲烷 | 点燃,观察火焰颜色 |
| C | 一氧化碳和二氧化碳气体 | 闻气味 |
| D | 木炭粉和氧化铜粉末 | 看颜色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
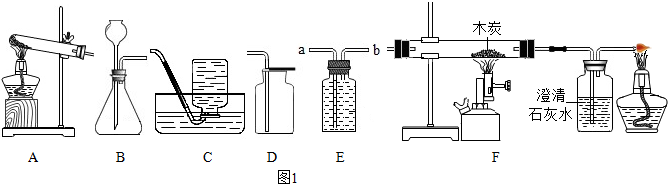

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com