
分析 因为化学方程式中各物质都是纯净物,所以在进行含杂质的物质根据化学方程式的计算时要注意是“纯量带入”,即把不纯的物质转化为纯物质带入求算,可以据此解答.
解答 解:设3000t这种矿石,可炼出生铁质量为x,
根据题设:纯Fe2O3质量=600t×80%=4800t
纯Fe质量=x•(1-4%)=x•96%
代入化学方程式中:
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
480t x•96%
$\frac{160}{480t}=\frac{112}{x•96%}$
x=350t
答:可炼出含杂质4%的生铁350t.
点评 含杂质的物质根据化学方程式的计算,关键是要把不纯物质转化为纯物质后再带入进行求算,转化公式为:纯物质的质量=不纯物质的质量×纯度


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一个偏二甲肼分子中含有一个氮气分子 | |
| B. | 由碳、氢、氮三种元素组成 | |
| C. | 是化合物 | |
| D. | 组成偏二甲肼的碳、氢、氮元素的质量比为6:2:7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
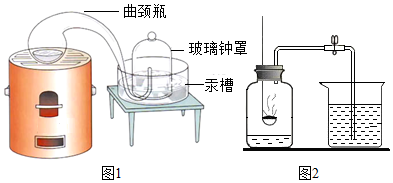
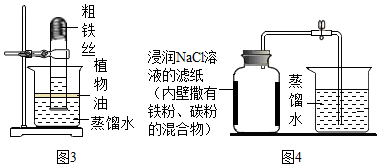
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 130mL | 90.0mL | 63.6mL |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
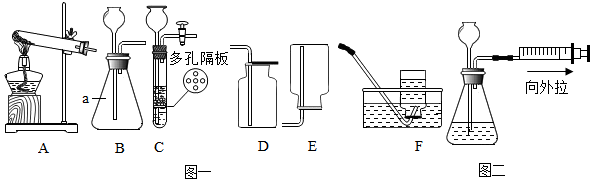
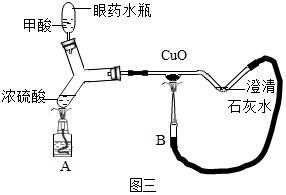
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
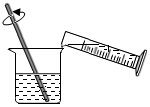 如图是稀释浓硫酸实验的示意图.
如图是稀释浓硫酸实验的示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com