
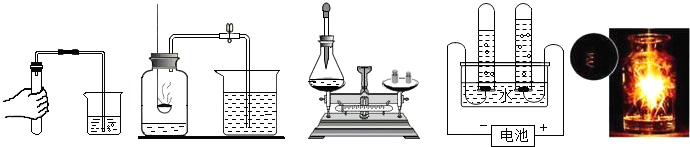
分析 (1)根据实验室制备气体时的步骤进行分析;
(2)根据测定空气中氧气的体积分数的实验原理、装置的特点、实验注意事项等,分析造成测得氧气的体积分数小于五分之一的因素可能有:1、装置是否漏气;2、红磷的用量是否充足;3、装置是否冷却到室温等;
(3)根据做验证质量守恒定律的实验时选用药品和装置特点分析;
(4)根据在电解水实验中正氧负氢,氢二氧一分析;
(5)根据铁丝在氧气中燃烧试验的注意事项分析.
解答 解:(1)实验室制取气体时,组装好装置后,应在向容器中装入药品前检查装置气密性,然后再装入药品;
(2)根据在测定空气中氧气的体积分数时注意事项:装置的气密性要好;为了要耗尽瓶中的氧气,红磷必须是足量的;气体的体积受到温度的影响,要等到装置冷却至室温,再打开弹簧夹等;因此可知达不到瓶中空气总体积的五分之一的原因可能是:装置漏气、红磷量不足、或没有等到冷却至室温,打开弹簧夹等;
(3)C实验用来验证质量守恒定律;
(4)在电解水实验中,正极产生的气体是氧气,负极产生的气体是氢气,且负极产生的气体体积是正极的二倍,简记为:正氧负氢,氢二氧一.所以在电解水实验中所产生氧气的体积是20mL,产生氢气的体积应该是40mL;
(5)铁在氧气中燃烧生成了四氧化三铁,放出大量的热,为了防止溅落的熔化物炸裂瓶底,在集气瓶底预先放少量水;
故答案为:(1)检查装置的气密性;(2)红磷量不足;(3)质量守恒;(4)40mL;(5)防止高温熔化物溅落,炸裂瓶底.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com