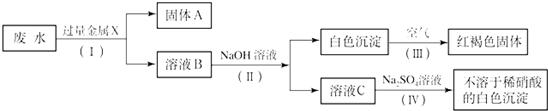
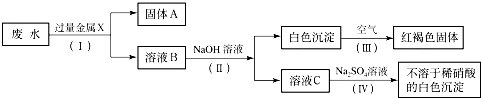
向某盐溶液中加入足量的NaOH溶液,生成红褐色沉淀,过滤后,向滤液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则该盐的化学式为( )
A.CuSO4
B.AgNO3
C.Fe2(SO4)3
D.Na2SO4
【答案】分析:红褐色沉淀是氢氧化铁,所以该盐溶液是铁盐溶液,不溶于稀硝酸的白色沉淀有硫酸钡沉淀和氯化银沉淀,再根据向滤液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀确定出白色沉淀的名称,进而推出盐的化学式.
解答:解:因为氢氧化铁沉淀是红褐色,所以该盐溶液中含有铁离子;向滤液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,因为不溶于稀硝酸的白色沉淀有硫酸钡沉淀和氯化银沉淀,要想生成氯化银沉淀,滤液中必须含有银离子,由题意可知反应后的溶液中阳离子是钠离子,所以不可能是氯化银沉淀,只能是硫酸钡沉淀,加入氯化钡溶液生成硫酸钡沉淀,说明滤液中含有硫酸根离子,即盐溶液中含有硫酸根离子,所以该盐是硫酸铁.
故选C.
点评:解答本题关键是要知道氢氧化铁是红褐色沉淀,推出盐中含有铁离子,要知道不溶于稀硝酸的白色沉淀有硫酸钡沉淀和氯化银沉淀,加入氯化钡生成氯化银沉淀,滤液中需要含有银离子,如果生成硫酸钡沉淀,滤液中需要含有硫酸根离子,再具体进行分析.