
“五水共治,治污为先”是我省提出改善生态环境的一项重要政策,为了防止水体污染,你认为下列措施中不可行的是( )
A. 不任意排放生活污水 B. 禁止使用农药和化肥
C. 工业污水经净化处理后再排放 D. 牲畜粪便适当处理后再施用
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
根据基础实验“配置一定溶质质量分数的氯化钠溶液”,填写相关实验内容:
(1)实验目的:配置25g溶质质量分数为20%的氯化钠溶液,…
(2)实验用品:食盐,蒸馏水等;
(填一种仪器名称)药匙,烧杯,玻璃棒,量筒,胶卷滴管,纸片等
(3)实验过程
①计算 ② (填一个操作步骤) ③量取水 ④溶解 ⑤转移
(4)实验回顾:
①通过计算可知,需要蒸馏水的体积为 mL.
②用量筒量取所需体积的蒸馏水时,下面读数方法正确的是 (填字母).
③溶解时用玻璃棒不断搅拌,目的是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
2013年1月,我省发布了环境空气质量指数(AQI),参与空气质量评价的主要污染物为PM10、PM2.5、…等6项指标,在发布的6项指标中,不包括下列哪种物质( )
A. SO2 B. NO2 C. CO2 D. CO
查看答案和解析>>
科目:初中化学 来源: 题型:
实验室制氧气的两种方法如下:
方法一:2H2O2 2H2O+O2↑
2H2O+O2↑
方法二:2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
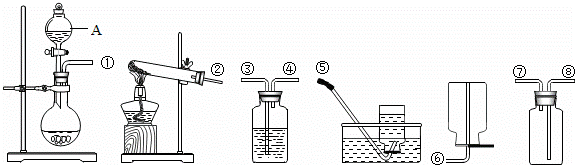
(1)两种方法涉及到的化学反应基本类型都是 _________ 反应;
(2)如图是实验室用于制取、干燥和收集气体的装置图,图中仪器A的名称是 _________ .现用方法一制取并收集一瓶干燥的氧气,请按气体流向,用导管的编号将装置连接好 _________ .
查看答案和解析>>
科目:初中化学 来源: 题型:
小科为研究“碱与盐反应”的规律,设计了如图所示的五组实验,每支试管盛有3毫升溶液,分别向试管中滴加3滴溶液,除氢氧化钙溶液是饱和外,其余溶液的质量分数都为5%,下列叙述正确的是( )
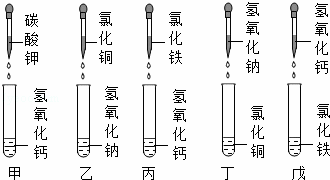
A. 甲组和乙组实验能观察到相同的现象
B. 乙组和丙组实验均能观察到蓝色沉淀
C. 乙组实验产生的沉淀质量比丁组多
D. 戊组实验产生的沉淀质量比丙组少
查看答案和解析>>
科目:初中化学 来源: 题型:
某实验小组利用下面装置制取二氧化碳气体并验证二氧化碳的部分性质,请回答:

⑴实验室欲制取一瓶二氧化碳气体,应选用装置是 ▲ ,有关化学方程式为 ▲ ;要得到干燥的二氧化碳气体,还应用到装置 ▲ 。
⑵一同学利用装置C验证制得的气体 时未看到浑浊现象,可能的原因是 ▲ 。要吸收反应多余的二氧化碳最好使用装置D而不用装置C,是因为 ▲ 。
时未看到浑浊现象,可能的原因是 ▲ 。要吸收反应多余的二氧化碳最好使用装置D而不用装置C,是因为 ▲ 。
⑶某同学将CO2通入紫色石蕊试液中,发现石蕊试液变红色
【提出问题】变红的是碳酸还是二氧化碳?
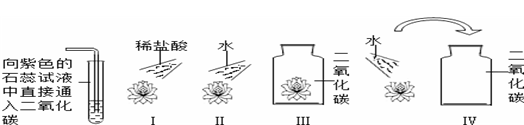 【猜想假设】:①是CO2;②是水;③是水与二氧化碳反应生成的碳酸.
【猜想假设】:①是CO2;②是水;③是水与二氧化碳反应生成的碳酸.
【实验探究】他用四支用紫色石蕊试液浸泡过的小纸花,晾干后,分别做了如下实验:
a.实验 Ⅰ中小花的颜色 ▲ 变红,Ⅱ、Ⅲ中小花的颜色不变,实验Ⅳ中小花的颜色 ▲ 。
Ⅰ中小花的颜色 ▲ 变红,Ⅱ、Ⅲ中小花的颜色不变,实验Ⅳ中小花的颜色 ▲ 。
b.做实验Ⅰ的目的是 ▲ 验证紫色石蕊试液遇酸性溶液变红色;做实验Ⅱ、Ⅲ的目的是 ▲ 。
通过实验说明①②③三个假设正确的是 ▲ 。
【讨论交流】实验(Ⅳ)结束后,将纸花用酒精灯小心加热
烘烤后纸花又变紫,说明碳酸 ▲ 。 不稳定,受热易分解
【拓展延伸】小华同学利用右图装置也能验证使石蕊变色的
物质是碳酸 而不是二氧化碳,若甲中吸有水,乙中吸有
稀硫 酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,
烧杯 ②中盛有碳酸钠粉末。他应采取的实验操作是 ▲ 。(2分)
查看答案和解析>>
科目:初中化学 来源: 题型:
某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
【原理思路】利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
【实验分析】小科同学根据以上思路,设计了如图1的实验装置。
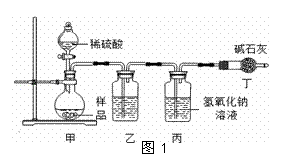 ①实验装置乙中盛放的试剂为 。
①实验装置乙中盛放的试剂为 。
装置丁中碱石灰的作用是 。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
 ②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的
质量分数 (填写“偏高”“偏低”或“不变”).
③小明同学认为小科的方案存在问题,即使操作规范下也会造成结果偏低,你
认为他的理由是 ,应该将装置甲中双孔橡
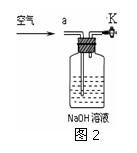
胶塞换成三孔橡胶塞,并增加图2装置,实验结束后缓缓通入一段时间空气,
目的是 ,其中NaOH溶液的作用是 。
(2)沉淀法.
【实验原理】利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
【实验步骤】①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即Na2CO3已完全反应)的方法是: 静置,向上层清液中滴加 溶液,如果没有白色沉淀生成,证明CaCl2过量;
③过滤、操作X、干燥、称量沉淀的质量为10.0g,操作X的名称是 ,如果缺少此操作会造成碳酸钠质量分数 (填写“偏高”“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数为 。(写出计算过程,结果保留至0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com