
分析 (1)根据分子之间有间隔进行分析;
(2)根据空气中各种气体的体积分数进行分析;
(3)根据原子得失去电子后会形成离子进行分析;
(4)根据水结冰后体积变大进行分析;
(5)根据两物质的化学式,由组成元素的质量分数计算公式,计算出两物质中碳元素的质量分数.
解答 解:(1)分子之间有间隔,所以液体体积:50mL酒精与50mL水混合>100mL;
(2)空气中各种气体的体积分数是稀有气体占0.94%,二氧化碳占0.03%,所以空气中气体的体积分数:稀有气体>二氧化碳;
(3)原子得失去电子后会形成离子,钠原子失去电子会形成钠离子,所以核外电子总数:钠原子(Na)>钠离子(Na+);
(4)水结冰后体积变大,所以分子间空隙大小:0℃时的水<0℃时的冰;
(5)CH2O中C元素的质量分数为$\frac{12}{30}$×100%=40%;葡萄糖(C6H12O6)中C元素的质量分数=$\frac{12×6}{180}$×100%=40%;所以两物质中含碳量相等.
故答案为:(1)>100mL;
(2)>;
(3)>;
(4)<;
(5)=.
点评 本题难度不大,考查知识比较全面,掌握分子间隔、核外电子排布、元素的质量分数等知识是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
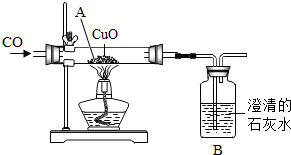 如图为一氧化碳还原氧化铜的装置图.
如图为一氧化碳还原氧化铜的装置图.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
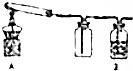 某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用如图所示装置进行实验,图中铁架台等装置已略去;反应一段时间后停止加热,冷却到室温,反应前、后测得的数据如下:
某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用如图所示装置进行实验,图中铁架台等装置已略去;反应一段时间后停止加热,冷却到室温,反应前、后测得的数据如下:| 装置 | 反应前 | 反应后 |
| A | 试管的质量38.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量56.8克 |
| B | 反应后瓶内石灰水比反应前增重1.1 克 | |
| A. | 装置中可能还有一部分CO2未被石灰水溶液吸收 | |
| B. | 氯化铜和炭粉反应产生的气体除CO2外还有CO | |
| C. | 氧化铜和炭粉可能没有完全反应 | |
| D. | 该反应不符合质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20℃时100克氯化钠溶液中含有36克氯化钠 | |
| B. | 20℃时100克氯化钠饱和溶液中含有36克氯化钠 | |
| C. | 20℃时100克水中达到饱和状态时能溶解36克氯化钠 | |
| D. | 20℃时氯化钠溶液中溶质的质量分数为36% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
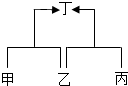 已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:
已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3↓+H2O 复分解反应 | |
| B. | 比较铜和银的金属活动性:Cu+2AgCl═2Ag+CuCl2置换反应 | |
| C. | 铝制品有很好的抗腐蚀性:4Al+3O2═2Al2O3 化合反应 | |
| D. | 工业上制氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ 分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com