
 在氢气还原氧化铜的实验中,向50克氧化铜粉末中通氢气,加热一段时间后,冷却测定固体质量42g,求:
在氢气还原氧化铜的实验中,向50克氧化铜粉末中通氢气,加热一段时间后,冷却测定固体质量42g,求:分析 (1)在加热条件下,氢气夺取氧化铜中的氧元素而变成水,氧化铜失去氧而变成铜;由于失去氧元素导致反应后残余固体质量减小;根据反应的化学方程式,利用反应前后固体物质的差量法,可由反应前后固体质量差计算参加反应的氧化铜的质量;
(2)根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%分析计算;
(3)根据浓盐酸和浓硫酸的性质解答.
解答 解:(1)根据题意,减少的元素的质量为50g=42g=8g
设参加反应的氧化铜的质量为x
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O 固体质量减少
80 64 80-64=16
x 8g
$\frac{80}{16}=\frac{x}{8g}$
x=40g
(2)溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%=$\frac{50mL×1.84g/mL×98%}{50mL×1.84g/mL+300mL×1g/mL}$×100%=23%;
(3)浓盐酸具有挥发性,能挥发出溶质氯化氢从而与空气中的水蒸气结合产生盐酸的小液滴,形成白雾,而浓硫酸不具有挥发性,打开瓶塞没有现象;
故答案为:(1)40g;(2)23%;(3)浓盐酸挥发形成白雾,而浓硫酸打开瓶塞没有现象.
点评 根据反应前后固体质量差即氧化铜中氧元素的质量,因此可根据氧化铜中氧元素的质量分数计算氧化铜的质量.


科目:初中化学 来源: 题型:填空题
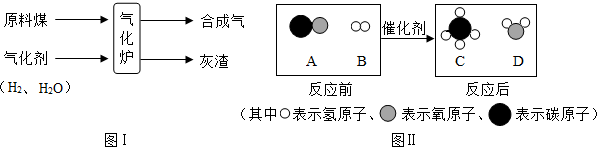
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1:1 | B. | $\frac{n-4}{6-n}$ | C. | $\frac{4-n}{6-n}$ | D. | $\frac{1}{m}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然界有单质M存在,无单质N,则N>M | |
| B. | 金属M、N的薄片与同样的稀盐酸反应,其中M中产生氢气更快,则M>N | |
| C. | M的化合物的溶液不能用N制的容器盛放,但可用Q制的容器盛放,则M>N>Q | |
| D. | 因为H>Cu,所以反应“H2+CuO$\frac{\underline{\;加热\;}}{\;}$Cu+H2O”能够发生 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
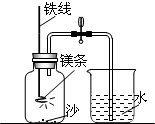 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 小明在实验手册上看见了如图所示的装置图,实验现象一栏写着:“黑色固体变红,澄清石灰水变浑浊”
小明在实验手册上看见了如图所示的装置图,实验现象一栏写着:“黑色固体变红,澄清石灰水变浑浊”查看答案和解析>>
科目:初中化学 来源: 题型:解答题
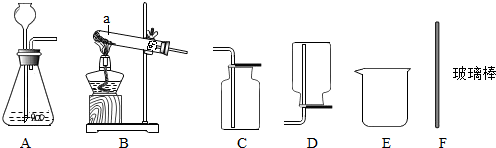
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com