

分析 (1)根据制取氨气的反应,写出反应的化学方程式;
(2)反应物的状态、反应条件、气体的密度、溶解性等是选择的依据;
解答 解:(10实验室里加热氯化铵(NH4Cl)和熟石灰两种固体的混合物可制取氨气,同时生成氯化钙和水.反应的化学方程式是:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)实验室制取气体,气体的发生装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.由上述分析可知,因制取氨气是固固混合,反应条件是加热,发生装置选择A,密度比空气小,极易溶于水,收集装置选择C,用生石灰与浓氨水混合快速制取大量的氨气,为固液常温反应,发生装置选择B.
故答案为:(1)2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;(2)A、C、B.
点评 本题的难度不大,熟练掌握实验室制取气体的制法是解答本题关健.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④ | C. | ①②④ | D. | ②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 操作一:取小苏打样品少量溶于足量水后,加入过量的②(填药品编号,下同),观察,如有沉淀,则继续进行下一步操作; 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的④,观察. | 操作一中无沉淀出现 | 假设一成立 |
| 操作一中有沉淀出现 | 假设二成立 | |
| 操作二中产生气泡 | 假设三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| X | Y | Z | W | |
| 盐酸 | √ | ─ | ─ | √ |
| Z的硝酸盐 | √ | |||
| W的硝酸盐 | √ | ─ |
| A. | X>Y>W>Z | B. | W>X>Y>Z | C. | X>W>Y>Z | D. | Y>W>Z>X |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
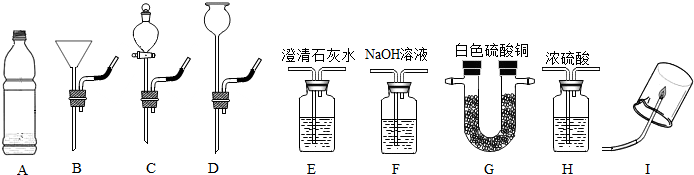
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
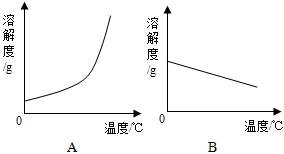 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子一定都是由原子核和核外电子构成的 | |
| B. | 化学变化中元素种类一定不变化 | |
| C. | 最外层电子数为8的粒子一定是稀有气体的原子 | |
| D. | 物理变化中分子种类一定不变化 |
查看答案和解析>>
科目:初中化学 来源:2017届山东省菏泽市九年级中考预测题(一)化学试卷(解析版) 题型:信息分析题
甲、乙、丙、丁均为中学化学中的常见物质,其中甲是大理石的主要成分,乙是造成温室效应的主要气体,它们之间的转化关系如图所示。请根据相关信息回答问题:
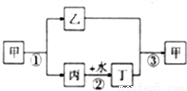
(1)写出物质甲的化学式;_______.丙的俗名_______;
(2)写出反应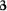 的化学方程式 ____________________________,该反应是二氧化碳的鉴别中发生的反应,对于鉴别过程中发生的现象的描述是________________;
的化学方程式 ____________________________,该反应是二氧化碳的鉴别中发生的反应,对于鉴别过程中发生的现象的描述是________________;
(3)上述四种物质中的一种常和___________ (填物质的名称)用于实验室制取二氧化碳。
查看答案和解析>>
科目:初中化学 来源:2017届上海市杨浦区九年级4月学业质量调研化学试卷(解析版) 题型:信息分析题
用下图常用实验装置制取常见的气体,并进行相应性质实验。
实验一:实验室中可用KClO3在MnO2催化下受热分解制取氧气,完全反应后对混合物进行分离回收并进行相关性质实验,实验操作如图所示(MnO2难溶于水)。
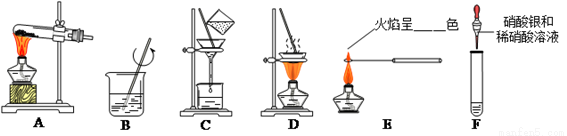
(1)写出图A中发生反应的化学方程式_____________________________。图B操作的名称是___________,图C操作中的一处明显错误是___________________________________,图D操作中,当看到_________________________时停止加热。
(2)取C中滤液分别进行如图E、F所示实验,E处透过蓝色钴玻璃观察火焰呈_______色,F中滴加硝酸银和稀硝酸产生的实验现象是___________________。
实验二:
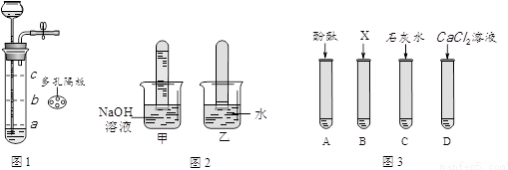
(1)若用图1装置制取二氧化碳气体,为了便于控制反应随时发生和停止,多孔隔板合适的 位置是________处(选填“a”、“b”或“c”),不适宜用作多孔隔板的材料是_________。
A.铁 B.塑料 C.铜片 D.石墨
(2)用图1装置制取并收集两试管CO2气体,分别倒扣入图2盛有等体积NaOH溶液和水的 烧杯中,该组对比实验产生的现象说明_______________________________。
(3)为了进一步探究CO2与NaOH溶液是否发生反应,取图2甲烧杯实验后的溶液于图3(A~D)四支试管中,分别滴入四种不同类别的试剂,B中加入的是_________。四种方案中不合理的是______________,理由是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com