
| A. | 干冰、碳酸、苛性钠、小苏打、空气 | |
| B. | 五氧化二磷、醋酸、氢氧化钙、硝酸镁、酒精 | |
| C. | 氯酸钾、硝酸、氢氧化铜、硫酸亚铁、天然气 | |
| D. | 生石灰、磷酸、纯碱、氯化钠、石油 |
分析 根据氧化物、酸、碱、盐、混合物的特点分析即可:氧化物是由两种元素组成并且一种元素是氧元素的化合物;电离时生成的阳离子都是氢离子的化合物是酸;电离时生成的阴离子都是氢氧根离子的化合物是碱;由金属离子和酸根离子组成的化合物是盐;混合物是由多种物质组成的物质.据此逐项分析判断即可.
解答 解:A、干冰属于氧化物,碳酸属于酸,苛性钠属于碱,小苏打属于盐,空气属于混合物.故选项正确;
B、五氧化二磷属于氧化物,醋酸属于酸,氢氧化钙属于碱,硝酸镁属于盐,酒精属于纯净物.故选项错误;
C、氯酸钾属于盐,硝酸属于酸,氢氧化铜属于碱,硫酸亚铁属于盐,天然气属于混合物.故选项错误;
D、生石灰是氧化钙属于氧化物,磷酸属于酸,纯碱、氯化钠属于盐,石油属于混合物.故选项错误.
故选A.
点评 本题主要考查物质分类的知识,解答时要分析物质的元素组成,然后再根据酸碱盐概念、特征进行分析、判断;解题时可用排除法排除不符合题意的选项.


科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 所选试剂及操作方法 |
| A | 除去二氧化碳中的少量一氧化碳气体 | 通入氧气、点燃 |
| B | 除去氯化钾中的二氧化锰 | 加水溶解、过滤、蒸发 |
| C | 除去氧化钙中的碳酸钙 | 加水溶解、过滤 |
| D | 除去稀盐酸中的稀硫酸 | 加入足量的氢氧化钡溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
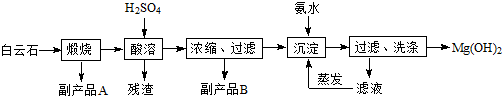
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
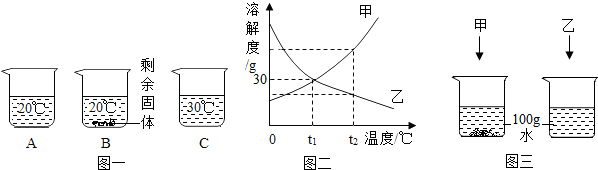
 化学上通常用溶解度来定量表示某种物质在某种溶剂中的溶解性.右图为KNO3和 NaCl两种物质的溶解度曲线.
化学上通常用溶解度来定量表示某种物质在某种溶剂中的溶解性.右图为KNO3和 NaCl两种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含有3个质子,没有中子 | B. | 含有2个质子,1个中子 | ||
| C. | 含有1个质子,2个中子 | D. | 含有3个中子,没有质子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
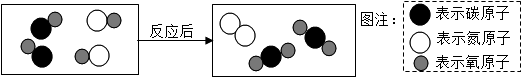
| A. | 参加反应的物质分子个数比为1:1 | |
| B. | 该反应为置换反应 | |
| C. | 生成物的质量比为7:22 | |
| D. | 反应物均为氧化物且该反应遵循质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com