
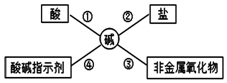
分析 (1)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水;
(2)碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能使酚酞试液变红色,能和氯化钙反应生成碳酸钙沉淀和氯化钠,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;
(3)显碱性溶液能使酚酞试液变红色,是因为显碱性溶液中都含有自由移动的氢氧根离子;
(4)硫酸属于酸,氯化钡属于盐,不能和氢氧化钾反应,硫酸铜属于盐,能和氢氧化钾反应生成氢氧化铜沉淀和硫酸钾,碳酸钠属于盐,不能和氢氧化钾反应.
解答 解:(1)如果该溶液变质,说明氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,发生反应的化学方程为:CO2+2NaOH═Na2CO3+H2O.
故填:CO2+2NaOH═Na2CO3+H2O.
(2)碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能使酚酞试液变红色,能和氯化钙反应生成碳酸钙沉淀和氯化钠,能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,而氢氧化钠溶液也能使酚酞试液变红色,因此要检验该氢氧化钠溶液已变质,选择下列试剂不能达到的是酚酞试液.
故选:B.
(3)为了验证反应④,小丽将无色酚酞试液分别滴入氢氧化钠溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中都能解离出OH-.
故填:OH-.
(4)硫酸属于酸,氯化钡属于盐,不能和氢氧化钾反应,硫酸铜属于盐,能和氢氧化钾反应生成氢氧化铜沉淀和硫酸钾,碳酸钠属于盐,不能和氢氧化钾反应,因此依据反应②,氢氧化钾能与下列物质反应的是硫酸铜,反应的化学方程式为:2KOH+CuSO4═K2SO4+Cu(OH)2↓.
故填:C;2KOH+CuSO4═K2SO4+Cu(OH)2↓.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
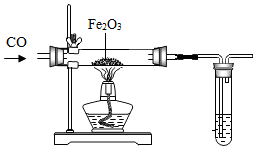 冶炼金属通常是指从矿石中提取金属单质的过程,除“沙土淘金”等物理方法外,金属冶炼大都是使金属从其化合态(化合物)转化为游离态(单质)的化学过程.根据金属的化学性质不同,工业上冶炼金属一般有以下几种方法.
冶炼金属通常是指从矿石中提取金属单质的过程,除“沙土淘金”等物理方法外,金属冶炼大都是使金属从其化合态(化合物)转化为游离态(单质)的化学过程.根据金属的化学性质不同,工业上冶炼金属一般有以下几种方法.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO | B. | K2S | C. | NO | D. | SO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4 KNO3 HCl Na2SO4 | B. | NaOH NaCl HCl FeCl3 | ||
| C. | NaNO3 HCl Na2SO4 H2SO4 | D. | K2CO3 H2SO4 CaCl2 Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 制备气体时,先装药品,后检查装置的气密性 | |
| B. | 用排水法收集完氧气,先把导管移离水面,后停止加热 | |
| C. | 用量筒量取10mL液体时,先倒入接近10mL的液体,后用胶头滴管补至刻度线 | |
| D. | 以上说法都不对 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 是一种氧化物 | |
| B. | 由C、H、O三种元素组成 | |
| C. | 由2个碳原子、2个氧原子和4个氢原子构成 | |
| D. | 相对分子质量为60g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
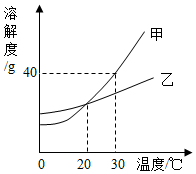 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 30℃时,甲的饱和溶液溶质质量分数为40% | |
| B. | 20℃时,甲、乙的饱和溶液中所含溶质的质量一定相等 | |
| C. | 将等质量的甲、乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙 | |
| D. | 将20℃时甲、乙的饱和溶液升温到30℃,所得甲、乙溶液的溶质质量分数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com