
科目:初中化学 来源: 题型:选择题
| A. | 石灰石、烧碱、氯化钙 | B. | 植物油、酒精、浓硫酸 | ||
| C. | 硫酸亚铁、氧化钙、氯化镁 | D. | 硫酸铝、氯化钠、硝酸钾 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
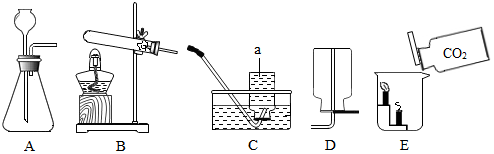
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
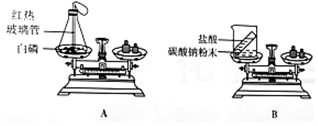
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
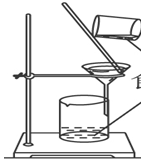 进行过滤实验验时必须注意“一贴、二低、三靠”.一贴:滤纸要紧贴漏斗壁;
进行过滤实验验时必须注意“一贴、二低、三靠”.一贴:滤纸要紧贴漏斗壁;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 用如图所示装置进行实验.A的容积为350mL,装置气密性良好,实验前K1、K2均已关闭.
用如图所示装置进行实验.A的容积为350mL,装置气密性良好,实验前K1、K2均已关闭. | A. | ①②③④⑤⑥ | B. | ②③④⑤⑥ | C. | ②③④⑤ | D. | ①③④⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 医疗上用氧气进行急救 | B. | 氧炔焰用来焊接或切割金属 | ||
| C. | 液氧可用作火箭燃料 | D. | 制成液氧炸药,用来开山采矿 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe+H2SO4(浓)═FeSO4+H2↑ | |
| B. | Al2O3+6HCl═2AlCl3+3H2O | |
| C. | NaOH+H2SO4═NaSO4+H2↑ | |
| D. | BaSO4+2HNO3═Ba(NO3)2═Ba(NO3)2+H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com