
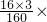 100%=30%、
100%=30%、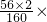 100%=70%.
100%=70%. 100%=x×70%,x=48g.
100%=x×70%,x=48g.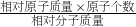 ×100%,进行分析解答.
×100%,进行分析解答.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源:不详 题型:单选题
| A.两个氧分子:O2 |
| B.水通电得到氧气的化学方程式是2H2O=O2↑+2H2↑ |
| C.CO2中氧元素的化合价为+2价 |
| D.氢氧化铁的化学式:Fe(OH)3 |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省常州市西藏民族中学九年级(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源:2011-2012学年云南省昭通市鲁甸县茨院中学九年级(上)期末化学试卷(解析版) 题型:选择题
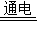 O2↑+2H2↑
O2↑+2H2↑查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com