



 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| 实验事实 | 数据分析及结论 | ||||||||
| 1.8g葡萄糖完全燃烧, 得到2.64g CO2和1.08g H2O |
数据分析: 若葡萄糖中只含有C、H两种元素,则需O2:2.64g+1.08g-1.8g=1.92g,而2.64gCO2中氧的质量为2.64g×
若葡萄糖中只含有C、H两种元素,则需O2:2.64g+1.08g-1.8g=1.92g,而2.64gCO2中氧的质量为2.64g× ;
结论:葡萄糖含有C、H、O三种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| MnO2与KClO3的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1LO2所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
查看答案和解析>>
科目:初中化学 来源:2012-2013学年江苏省江阴市九年级10月考化学试卷(解析版) 题型:填空题
人类的生存离不开氧气.某校化学兴趣小组的同学在老师的指导下做了有关氧气的系列探究实验:
探究一:以下是该小组探究影响H2O2溶液反应速率部分因素的相关实验数据.
|
实验序号 |
H2O2溶液 浓度% |
H2O2溶液 体积/mL |
温度/℃ |
MnO2的 用量/g |
收集氧气的 体积/mL |
反应所需 的时间/s |
|
① |
5 |
1 |
20 |
0.1 |
4 |
16.75 |
|
② |
15 |
1 |
20 |
0.1 |
4 |
6.04 |
|
③ |
30 |
5 |
35 |
0 |
2 |
49.21 |
|
④ |
30 |
5 |
55 |
0 |
2 |
10.76 |
⑴ 写出实验室用H2O2溶液和MnO2混合制氧气的文字或符号表达式: 。
⑵ 通过实验①和②对比可知,化学反应速率与 有关;
从实验③和④对比可知,化学反应速率与温度的关系是: 。
⑶ 通过上述实验 (填“能”或“不能”)说明使用MnO2可以加快H2O2溶液反应速率.
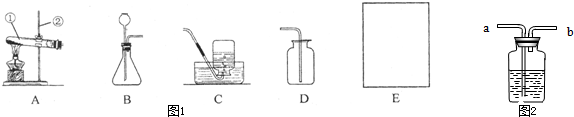
探究二:某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
已知:在空气中,温度超过40℃,白磷(化学符号为P)就可以自燃,即和氧气反应生成五氧化二磷。
如图是“空气中氧气体积分数测定”实验的改进装置.主要操作是:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃.

⑴请写出白磷与氧气反应的文字或符号表达式
⑵ 白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是 ;若实验非常成功,最终集气瓶中水的体积约为 mL.
⑶ 集气瓶里预先装进的50mL水,在实验过程中起到哪些作用? (填写序号)
a.加快集气瓶冷却
b.液封导气管末端以防气体逸出
c.缓冲集气瓶内气压的骤然升高.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com