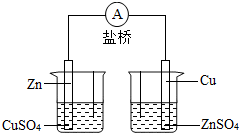
分析:A、根据原电池原理分析.正极得电子,负极失去电子;电池反应为氧化还原反应;盐桥的作用就是使电荷守恒,形成闭合回路,阳离子向正极移动,阴离子向负极移动.
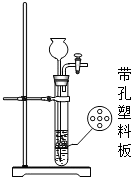
B、根据导气管不应该深入液面以下进行解答;
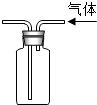
C、根据氢气的密度小于空气的密度进行解答;
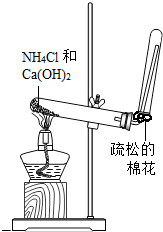
D、根据氯化铵和氢氧化钙反应生成氨气以及氨气的密度小于空气的密度进行解答.
解答:解:A、电池反应原理为锌与硫酸铜溶液反应置换铜,所以应该是锌放在硫酸锌溶液中,而铜放在硫酸铜溶液中,故A错误.
B、导气管不应该深入液面以下,以有利于气体逸出,故B错误;
C、氢气的密度小于空气的密度,所以收集氢气应短管进长管出,故C正确;
D、氯化铵和氢氧化钙反应生成氨气,氨气的密度小于空气的密度,用向下排空气法收集,故D正确.
故选:CD.
点评:对熟悉的实验进行再现式考查,解答时要注意实验中是否出现与所熟悉的实验有所不同,避免忽略了小的改变而出现误判.