
| A. | 镁带燃烧 Mg+O2↑$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| B. | 除去CO2中的CO CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | |
| C. | 用稀盐酸除铁锈 Fe2O3+6HCl═2FeCl3+3H2O | |
| D. | 用燃烧的方法测定空气中氧气的含量 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:A、该化学方程式氧化镁的化学式书写错误,氧气是反应物,后面不需要标注↑,正确的化学方程式应为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
B、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项错误.
C、该化学方程式书写完全正确.
D、铁在空气中不能燃烧,不能用于测定空气中氧气的含量,故选项错误.
故选:C.
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 为测定“碱”样品(主要成分为含少量NaCl的Na2CO3)中Na2CO3的含量,某化学课外活动小组的同学进行了以下探究:
为测定“碱”样品(主要成分为含少量NaCl的Na2CO3)中Na2CO3的含量,某化学课外活动小组的同学进行了以下探究:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石蕊试液和浓盐酸 | B. | 酚酞溶液和小苏打溶液 | ||
| C. | 石蕊试液和溶液硫酸 | D. | 酚酞溶液和浓氨水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
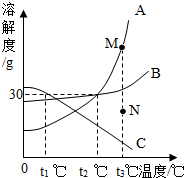
| A. | 若要将组成在N点的A溶液转变为M点的A溶液,可以采取恒温蒸发溶剂的方法 | |
| B. | t2℃时,A、C两种物质溶液的溶质的质量分数一定相等 | |
| C. | t2℃时,A、B两种物质的饱和溶液降温到t1℃,析出A的质量更大 | |
| D. | t3℃时,三种物质的溶质质量分数大小顺序为A>B>C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com