
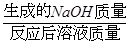 ×100%,反应后溶液的质量可根据质量守恒定律,由反应前混合物的质量总和减去生成的沉淀碳酸钙而求得,故只需要用碳酸钠的质量表示出生成的氢氧化钠的质量和形成沉淀的质量,即可利用反应后溶液中的溶质的质量分数的公式和质量守恒定律,计算出碳酸钠的质量,再使用溶质的质量分数计算公式计算出原碳酸钠溶液的溶质质量分数即可。
×100%,反应后溶液的质量可根据质量守恒定律,由反应前混合物的质量总和减去生成的沉淀碳酸钙而求得,故只需要用碳酸钠的质量表示出生成的氢氧化钠的质量和形成沉淀的质量,即可利用反应后溶液中的溶质的质量分数的公式和质量守恒定律,计算出碳酸钠的质量,再使用溶质的质量分数计算公式计算出原碳酸钠溶液的溶质质量分数即可。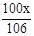
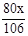
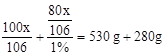
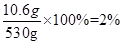


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| | 第一次 | 第二次 | 第三次 | 第四次 |
| 加稀盐酸的质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体质量(g) | 9.10 | 8.45 | 7.80 | 7.80 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
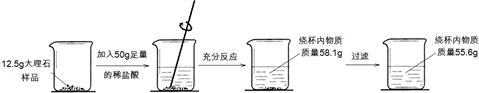
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
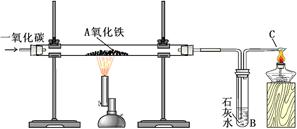
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 名 称 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 6.00 | 24.00 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.1﹕71 | B.2﹕71 | C.1﹕79 | D.2﹕79 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com