
【题目】是a,b,c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: 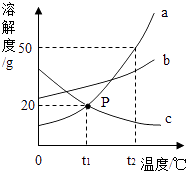
(1)P点的含义是
(2)t2℃时30g a物质加人到50g水中不断搅拌,能形成80g溶液吗?(填写“能”或“不能”).
(3)t2℃时a,b,c三种物质的溶解度按由小到大的顺序排列是(填写物质序号).
(4)将t1℃时a,b,c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是(填写选项序号).
A.c>a=b
B.a=b>c
C.a>b>c
D.b>a>c
(5)将t2℃时a,b,c三种物质饱和溶液的温度降到t1℃时,三种溶液的溶质质量分数大小关系是
(6)若A中混有B,得到A采用的结晶方法.
【答案】
(1)t1℃时,a、c两种物质的溶解度相等
(2)不能
(3)c<b<a
(4)D
(5)b>a>c
(6)降温结晶
【解析】解:(1)通过分析溶解度曲线可知,P点的含义是在t1℃时,a、c两种物质的溶解度相等;(2)t2℃时,a物质的溶解度是50g,30ga物质加人到50g水中不断搅拌,会溶解25g,能形成75g的饱和溶液;(3)通过分析溶解度曲线可知,t2℃时a,b,c三种物质的溶解度按由小到大的顺序排列是:c<b<a;(4)t1℃时,b物质的溶解度最大,a、c物质的溶解度相等,但是c物质的溶解度随温度的升高而减小,所以a,b,c三种物质饱和溶液的温度升高到t2℃时,b物质的溶质质量分数最大,a物质次之,c物质最小,故选:D;(5)在t2℃时,a物质的溶解度最大,b物质次之,c物质的溶解度最小,c物质的溶解度随温度的升高而减小,t1℃时,b物质的溶解度最大,a、c物质的溶解度相等,所以将t2℃时a,b,c三种物质饱和溶液的温度降到t1℃时,三种溶液的溶质质量分数大小关系是:b>a>c;(6)A物质的溶解度受温度影响较大,B物质的溶解度受温度影响较小,所以若A中混有B,得到A采用降温结晶的结晶方法.
所以答案是:(1)在t1℃时,a、c两种物质的溶解度相等;(2)不能;(3)c<b<a;(4)D;(5)b>a>c;(6)降温结晶.
【考点精析】解答此题的关键在于理解结晶的原理、方法及其应用的相关知识,掌握结晶的两种方法:蒸发溶剂,如NaCl(海水晒盐)和降低温度(冷却热的饱和溶液,如KNO3),以及对固体溶解度曲线及其作用的理解,了解1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).


科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具.
(1)用化学符号填空: ①碘原子②三个铁离子;
③两个三氧化硫分子; ④人体中含量最多的金属元素
(2)用字母序号填空:a.Ca(OH)2 b.H2 c.C6H12O6 d.KMnO4①可用于实验室制氧气的是; ②可用于改良酸性土壤的是;
③可用作清洁能源的是; ④医学上称为“低血糖”中的糖是;
(3)写出下列反应的化学方程式: ①烧碱在空气中变质; ②电解水
③工业炼铁原理; ④加热氯酸钾和二氧化锰的混合物 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图. 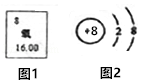
(1)在元素周期表中,氧元素的原子序数为 .
(2)图2所示粒子为(填“离子”或“原子”).
(3)由氧元素组成的一种气体单质可以支持燃烧,写出实验室制取该气体的一个化学方程式
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学要用含CaCO380%的大理石与足量的稀盐酸反应制备1000mL标准状况下的二氧化碳气体.己知标准状况下的二氧化碳气体的密度为:1.98g/L.假设大理石中的杂质不与稀盐酸反应,计算该同学最少需要准备多少克大理石.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用如图装置进行气体的制取实验,请回答下列问题: 
(1)写出标号a仪器的名称: .
(2)用氯酸钾制取氧气的化学方程式 , 选择④装置收集氧气,气体从(填字母)端进入.若改用排水法收集,实验结束后先撤导气管后熄灭酒精灯,目的是防止 .
(3)实验室用大理石和(填写药品名称)反应制取二氧化碳.与②相比,③作为发生装置的优点是 , 在装置④中盛放可用于干燥二氧化碳气体.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸奶中含有的乳酸对健康是有益的,乳酸的化学式为(C3H6O3)。请计算:
(1)乳酸中碳、氢、氧元素的质量比为 (填最简整数比)。
(2)18g乳酸中氧元素的质量为 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电解食盐水可得到烧碱、氯气(Cl2)和一种可燃性气体,反应的化学方程式为;配制质量分数为5%的氯化钠溶液,若量取水时俯视量筒刻度读数(其他操作正确),溶液的质量分数5%(填“大于”、“小于”或“等于”);现有NaCl和NaBr的混合物共2.2g,溶于水并加入过量的AgNO3溶液后,生成AgCl和AgBr沉淀共4.75g,则原混合物的含钠元素的质量为g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com