
分析 (1)根据锌与稀硫酸在常温下反应分析回答;
(2)根据确定发生装置需要考虑的两种因素分析判断;
(3)根据常用仪器的用途分析回答;
(4)根据氢气的性质和常用仪器的用途分析回答.
解答 解:(1)由于锌与稀硫酸在常温下反应,从节约能源角度考虑,你将会选择方案是锌与稀硫酸来制取氢气,该方案的反应符号表达式为:Zn+H2SO4═ZnSO4+H2↑.
(2)实验室制取气体时,确定发生装置需要考虑的两种因素有反应物的状态和反应的条件;
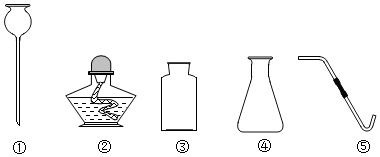
(3)由图示可知,仪器①的名称是长颈漏斗,酒精灯是常用的加热源,在该反应中不可能用到;
(4)由于氢气是密度最小的气体,难溶于水,可利用排水法或向下排空气法收集,根据以上仪器没中有水槽,确定该同学收集氢气的方法是向下排空气法收集.
故答为:(1)锌与稀硫酸,Zn+H2SO4═ZnSO4+H2↑.(2)AC;(3)长颈漏斗,酒精灯;(4)向下排空气法收集.
点评 本题的难度不大,了解实验室制取氢气的原理、装置和常用仪器的用途即可分析回答


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 清澈的湖水是混合物 | |
| B. | 活性炭可用于净化湖水 | |
| C. | 检验湖水是硬水还是软水可用肥皂水 | |
| D. | 过滤可以除去湖水中的可溶性杂质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com