
| (18n+48)g |
| 18ng |
| 10-x |
| y |
| 24 |
| 9n |
| 10-x |
| y |
| ||
| ||
| (18n+48)g |
| 18ng |
| 10-x |
| y |
| 24 |
| 9n |
| 10-x |
| y |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
| A、利用木炭的还原性可将氧化铜冶炼成铜 |
| B、金刚石是天然存在最硬的物质,可用于钻探机的钻头 |
| C、利用活性炭的稳定性来吸附冰箱中的异味 |
| D、大气中二氧化碳的消耗途径主要是植物的光合作用 |
查看答案和解析>>
科目:初中化学 来源: 题型:
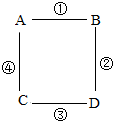 已知A、B、C、D四种物质是初中化学常见的不同类别物质.A为可溶性的碱,A、B、C中均含三种元素,反应①有两种沉淀生成.(“--”表示两种物质间能发生化学反应.)
已知A、B、C、D四种物质是初中化学常见的不同类别物质.A为可溶性的碱,A、B、C中均含三种元素,反应①有两种沉淀生成.(“--”表示两种物质间能发生化学反应.) 查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
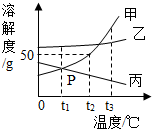 如图为甲、乙、丙三种物质的溶解度曲线示意图,根据图回答:
如图为甲、乙、丙三种物质的溶解度曲线示意图,根据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com